题目内容
【题目】下列说法不正确的是
A.用红磷测定空气中氧气含量时,红磷一定要过量
B.用排水法收集氧气时,导管口刚有气泡冒出就收集气体
C.硫粉在氧气中燃烧时,集气瓶中放少量水可吸收二氧化硫
D.实验室用过氧化氢制氧气的反应中,二氧化锰起催化作用
【答案】B
【解析】
试题分析:A、用红磷测定空气中氧气含量时,红磷一定要过量,以便将空气中的氧气完全消耗,正确,B、用排水法收集氧气时,一定要待导管口均匀冒出气泡才收集,刚有气泡冒出是装置内的空气,错误,C、因为二氧化硫有毒,故硫粉在氧气中燃烧时,集气瓶中放少量水可吸收二氧化硫,正确,D、实验室用过氧化氢制氧气的反应中,二氧化锰起催化作用,正确,故选B

 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型很多,如CaCO3、Al(OH)3、SiO2等。我校化学兴趣小组想探究牙膏摩擦剂的成分。
【提出问题1】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应;碱石灰由生石灰和氢氧化钠组成;氢氧化钡和氢氧化钙化学性质相似,也能与二氧化碳反应生成白色BaCO3沉淀和水。
【实验方案】取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,证明摩擦剂中含有 (填离子符号)。
【提出问题2】该牙膏中CaCO3的质量分数是多少?
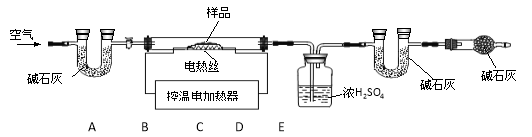
【实验装置】(不考虑装置内原有空气对实验的影响)
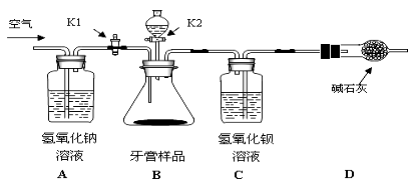
【实验步骤】
(1)按上图连接好装置后,发现一处明显的错误,改正为 ;
(2)重新连接好装置,并 ;
(3)在B装置中加入牙膏样品8.00g;
(4)关闭K1,打开K2,向牙膏样品中滴入10%的盐酸,至 ,停止滴加盐酸;
(5) ,至C中不再产生沉淀;
(6)将C装置中的固液混合物过滤、 、烘干后称量其质量;
(7)重复实验。
(已知此品牌牙膏中的摩擦剂为碳酸钙,且其他成分不和盐酸反应,装置内试剂均足量。)
【实验数据】重复实验,3次数据记录如下:
实验次数 | 实验1 | 实验2 | 实验3 |
C装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
【实验分析及数据处理】
(1)上述数据能否由托盘天平测得? 。(填“能”或“不能”)
(2)若没有A装置,则测定结果将 。(填“偏大”、“偏小”或“不变”)
(3)D装置的作用是 。
(4)据上表数据,计算该牙膏样品中CaCO3的质量分数?(写出计算过程,3分)
【实验反思】
(1)重复实验,取平均值的意义在于 。
(2)下列各项措施中,能提高测定准确度的是 (填序号)。
A.在装置A、B之间增加盛有浓硫酸的洗气瓶
B.在装置B、C之间增加盛有饱和碳酸氢钠的洗气瓶
C.缓缓滴加稀盐酸