题目内容
【题目】熟练掌握化学用语是学好化学的基础。用适当的化学用语填空:
(1)地壳中含量最多的金属元素_____;
(2)2个亚铁离子_____;
(3)n个二氧化氮分子_____;
(4)能保持氧气化学性质的微粒_____;
(5)标出二氧化硫中硫元素的化合价_____。
(6)2个硫酸根离子_____。
【答案】Al 2Fe2+ nNO2 O2 ![]() 2SO42-
2SO42-
【解析】
(1)地壳中含量最多的金属元素是铝元素,其符号为:Al;
(2)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个亚铁离子可表示为:2Fe2+;
(3)分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以n个二氧化氮分子可表示为nNO2;
(4)能保持氧气化学性质的微粒是氧分子,其化学式为:O2;
(5)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以标出二氧化硫中硫元素的化合价,故可表示为:![]() ;
;
(6)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个硫酸根离子可表示为:2SO42-。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如表.下列判断错误的是( )
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 8.8 | a |
A. X是生成物B. 表中a的值为2.8
C. X一定含有氧元素D. X可能含有氢元素
【题目】某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究。
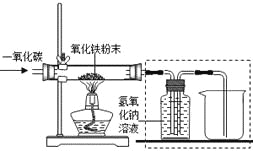
(设计实验)用一氧化碳还原纯净的氧化铁粉末,实验装置如下图。
(进行实验)该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
(分析与讨论)本实验中,玻璃管内固体粉末由红色全部变为黑色。小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料。
(查阅资料)①CO还原Fe2O3的固体产物的成分与反应温度、反应时间等因素有关;
②CO还原Fe2O3的实验过程中固体产物可能有Fe3O4、FeO、Fe;
③NaOH溶液与石灰水相似,能吸收CO2,但不变浑。
④
物质性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
颜色 | 黑色 | 黑色 | 红色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
(实验与猜想)
(1)该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和 。
(2)进行猜想:黑色固体粉末可能a.全部为铁、 b. 、c. 。
(得出结论)
(3)通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称) 。
(反思与评价)
(4)一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度。
(5)实验装置图中采用虚线框内的装置,其作用有 。
A.收集CO B.吸收CO2C.检验CO2
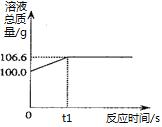
(实践应用)小明和他的同学想测定某赤铁矿石中Fe2O3的质量分数。用CO与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用足量的NaOH溶液完全吸收,该溶液总质量与反应时间的变化关系如右图。
(6)上述反应产生CO2的质量为 g;
(7)计算该赤铁矿石中氧化铁的质量分数。 。(需要有计算过程)