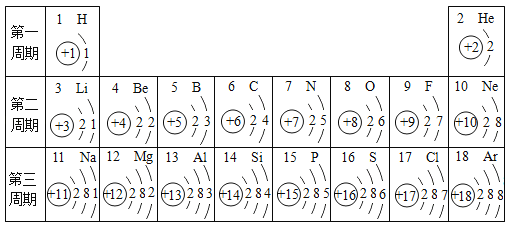
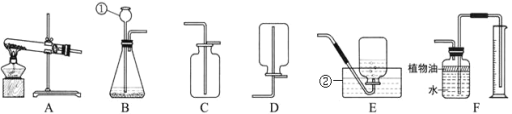
题目内容
【题目】将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如表.下列判断错误的是( )
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 8.8 | a |
A. X是生成物B. 表中a的值为2.8
C. X一定含有氧元素D. X可能含有氢元素
【答案】D
【解析】
本题主要考察质量守恒定律的相关知识
A、依据质量守恒定律,反应前的总质量=反应后的总质量,6.0+12.8=7.2+8.8+a则a=2.8,反应后a的质量变大,则a是生成物;故选项正确,不符合题意;
B、依据质量守恒定律,反应前的总质量=反应后的总质量,6.0+12.8=7.2+8.8+a则a=2.8;故选项正确,不符合题意;
C、丙醇中氧元素质量为6.0g×![]() ,氧气的质量为12.8g,反应物中氧元素总质量为1.6g+12.8g=14.4g。生成物中,二氧化碳中氧元素质量为8.8g×
,氧气的质量为12.8g,反应物中氧元素总质量为1.6g+12.8g=14.4g。生成物中,二氧化碳中氧元素质量为8.8g×![]() =6.4g,水中氧元素质量为:7.2g×
=6.4g,水中氧元素质量为:7.2g×![]() =6.4g,生成物中元素总质量为6.4g+6.4g=12.8g,反应物质氧元素总质量大于生成物中氧元素总质量,则a中一定含有氧元素;故选项正确,不符合题意;
=6.4g,生成物中元素总质量为6.4g+6.4g=12.8g,反应物质氧元素总质量大于生成物中氧元素总质量,则a中一定含有氧元素;故选项正确,不符合题意;
D、反应物中丙醇中氢元素质量为6.0g×![]() =0..8g,生成物中水中氢元素质量为7.2g×
=0..8g,生成物中水中氢元素质量为7.2g×![]() =0.8g,则a中不可能含有氢元素;故选项错误,符合题意;
=0.8g,则a中不可能含有氢元素;故选项错误,符合题意;
故选:D。

【题目】石灰石样品的主要成分是碳酸钙(已知其它杂质不与稀盐酸反应)。课外小组同学将50g稀盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入稀盐酸的质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体的质量/g | 16 | 12 | 8 | 4 | m |
请计算:
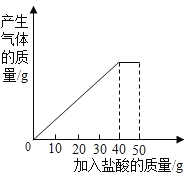
(1)m的值是______g.
(2)该样品中碳酸钙的质量分数为_________。
(3)求反应过程中产生二氧化碳的质量_________。(写出计算过程)