题目内容
【题目】有A、B、C、D四种元素,A元素的原子核内没有中子;B的次外层电子数占电子总数的1∕4;C的阳离子比B的原子多2个电子;D和C具有相同的电子层,D—的离子结构与氩原子结构相同。
(1)A元素的符号_______________;
(2)B原子的结构示意图_______________;
(3)C+的符号__________________;
(4)D—的结构示意图__________________________。
【答案】H 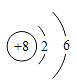 Na+
Na+ 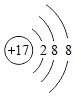
【解析】
根据“A元素的原子核内没有中子”,则推测A氢元素;根据“B的次外层电子数占电子总数的![]() ”,则推测B为氧元素;根据“C的阳离子比B的原子多2个电子;D和C具有相同的电子层,D—的离子结构与氩原子结构相同”,则推测C为钠元素,D为氯元素;代入检验,符合题意.
”,则推测B为氧元素;根据“C的阳离子比B的原子多2个电子;D和C具有相同的电子层,D—的离子结构与氩原子结构相同”,则推测C为钠元素,D为氯元素;代入检验,符合题意.
(1)由上分析可知A元素的符号H;
(2)B原子的结构示意图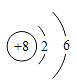 ;
;
(3)C+的符号Na+;
(4)D—的结构示意图 .
.
故答案为:(1)H;(2)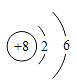 ;(3)Na+;(4)
;(3)Na+;(4) .
.

练习册系列答案
相关题目