题目内容
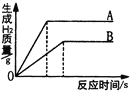
【题目】如图为甲,乙,丙三种物质的溶解度曲线.回答下列问题。
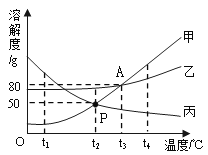
(1)t3℃时,甲物质的溶解度为___________________________________ 。
(2)配制等质量分数的甲,丙两物质的饱和溶液需控制的条件是____________________________ 。
(3)t1℃时,配制等质量的甲,乙,丙三种物质的饱和溶液,所需溶剂质量最多的为____________________________ 。
(4)将 t4℃时甲,乙,丙三种物质的饱和溶液降温至 t2℃,所得溶液的溶质质量分数由大到小的顺序为____________________________ 。
【答案】80g 温度为t2℃ 甲 乙>甲>丙
【解析】
(1)由溶解度曲线可知,t3℃时,甲物质的溶解度为80g;
(2)由甲、丙物质的溶解度曲线可知,在t2℃时甲、丙的溶解度相同,饱和溶液的浓度相同,所以配制等浓度的甲、丙两物质的饱和溶液,需控制的条件是温度为t2℃;
(3)由溶解度曲线的意义可知,t3℃时,甲物质的溶解度最小,所以配制等质量的甲、乙、丙三种物质的饱和溶液,所需溶剂质量最多的为甲;
(4)将t4℃时A、B、C三种物质的饱和溶液降温到t2℃时,甲、乙的溶解度减小,丙的溶解度随温度的降低而增大,甲、乙有晶体析出,质量分数变小,溶液仍为饱和溶液,丙没有晶体析出,质量分数不变,一定温度下饱和溶液的溶质分数=![]() ,溶解度越大,质量分数越大,t2℃时乙的溶解度大于甲的溶解度大于t4℃时丙的溶解度,所以t2℃时三种物质的溶质质量分数由大到小的顺序是乙>甲>丙。
,溶解度越大,质量分数越大,t2℃时乙的溶解度大于甲的溶解度大于t4℃时丙的溶解度,所以t2℃时三种物质的溶质质量分数由大到小的顺序是乙>甲>丙。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列叙述及对应的化学方程式、所属基本反应类型都正确的是( )
A | 洗去试管壁上附着的铜 | Cu+H2SO4=CuSO4+H2↑ | 置换反应 |
B | 酸雨的形成 | CO2 + H2O = H2CO3 | 化合反应 |
C | 用铁桶盛放稀盐酸 | Fe +2HCl=FeCl2+H2 ↑ | 置换反应 |
D | 拉瓦锡探究质量守恒定律 | 2HgO | 分解反应 |
A. AB. BC. CD. D
【题目】蜡烛(主要含 C,H,O 元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?亮亮同学认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:①燃烧的产物可能有CO2;②燃烧的产物可能有 H2O;除了上述猜想,你的猜想:燃烧的产物还可能有________________或_________________(填一种单质和化合物)
实验一:在密闭容器中点燃蜡烛至熄灭,抽取 10mL 密闭容器中的气体,注入到试管中的饱和澄清石灰水中,发现石灰水始终没有变浑浊.从实验的科学性考虑,下一步是____________(选填字母)
A直接得到燃烧产物中没有 CO2 的结论
B增加饱和澄清石灰水的质量
C再多抽取一些气体注入到试管中的石灰水中
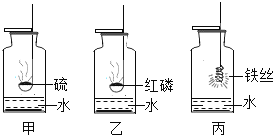
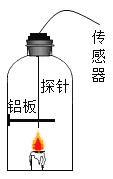
实验二:在老师的指导下,利用多功能传感器进行有关量的测量传装置如图所示.实验结束后,铝板表面有黑色固体颗粒,同时传感器采得实验前后的有关数据如表所示:
相对湿度 | 氧气含量 | 二氧化碳含量 | 一氧化碳含量 | |
蜡烛点燃前 | 48.4% | 18.7% | 0.058% | 0 |
蜡烛熄灭后 | 71.6% | 15.6% | 36.43% | 0.0182% |
由实验及结果分析,密闭容器内蜡烛熄灭的原因是_____________________,.蜡烛燃烧生成的产物是__________________________(填化学式)。