题目内容
 构建知识网络是学习和研究化学常用的科学方法.如图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D表示氧化物、酸、碱、盐的某一种,“-”表示物质之间能够发生化学反应.
构建知识网络是学习和研究化学常用的科学方法.如图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D表示氧化物、酸、碱、盐的某一种,“-”表示物质之间能够发生化学反应.
请按要求回答下列问题.
(1)从物质类别看,“A”物质属于______;“B”物质属于______.
(2)除去铁锈利用的反应是______(填序号,下同),实验室制取CO2利用的反应是______.
(3)举一例用化学方程式表示溶液质量减少的反应③______;举一例用化学方程式表示反应⑥______.
(4)反应④⑤⑥都是______反应,其实质是阴阳离子结合生成沉淀、气体或水,请回答反应⑤的实质是B、C在水中解离出的______(填化学符号)结合生成了______.
(5)请依据(4)中获得的启示,判断下列各组离子在水溶液中能大量共存的是______.
A.Ba2+、SO42- B.CO32-、H+ C.H+、OH- D.Na+、NO3-.
解:(1)盐的化学性质有四个:盐与金属反应、盐与酸反应、盐与碱反应、盐与盐反应.由题目给出的信息可知:“A”物质属于氧化物,“B”物质属于酸,因为金属既能与酸反应又能与盐溶液反应;
(2)由于工业上常用盐酸或硫酸出铁锈,应用盐酸除铁锈的反应的方程式是:Fe2O3+6HCl=2FeCl3+3H2O;实验室制取CO2反应物是碳酸钙和盐酸,生成物是氯化钙、水、二氧化碳,用观察法配平,所以方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)反应③是金属与盐反应,可以是铁和硫酸铜反应,生成铜和硫酸亚铁,方程式是:Fe+CuSO4=FeSO4+Cu;因为B是酸,酸与盐反应,可以是碳酸钙与盐酸反应,生成氯化钙、水、二氧化碳,用观察法配平,二氧化碳后面标上上升符号,所以方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)酸、碱、盐之间发生的化学反应都是复分解反应,反应⑤是酸和碱反应生成盐和水,反应的实质是酸电离出来的氢离子与碱电离出来的氢氧根离子结合生成水;
(5)各组离子在水溶液中能大量共存,相互之间结合不能生成沉淀,不能生成气体,不能生成水,A中生成硫酸钡沉淀,不能共存,B中生成水和二氧化碳,不能共存,C中生成水,不能共存,所以D答案正确.
故答案为:(1)氧化物;酸;(2)①;(3)Fe+CuSO4=FeSO4+Cu;CaCO3+2HCl═CaCl2+H2O+CO2↑;(4)复分解;H+、OH-;H2O;(5)D.
分析:盐的化学性质有四个:盐与金属反应、盐与酸反应、盐与碱反应、盐与盐反应.由题目给出的信息可知:“A”物质属于氧化物,“B”物质属于酸,因为金属既能与酸反应又能与盐溶液反应;从物质组成看,一定由三种元素组成的是碱;反应③是金属与盐溶液的反应,铁和硫酸铜溶液反应生成铜和硫酸亚铁,合理即可;反应⑥是酸与盐的反应,可以是碳酸钙与盐酸反应,合理即可;CaCl2溶液与Na2CO3溶液能够反应的实质是:它们在水中解离出的钙离子与碳酸根离子结合成了碳酸钙白色沉淀;在水溶液中能大量共存的是Na+、NO3-,因为它们相互间没有气体、沉淀或水生成,因此能大量共存.
点评:本题考查了盐的化学性质,解决本考点需要根据实验现象综合分析,从而得出正确的结论.
(2)由于工业上常用盐酸或硫酸出铁锈,应用盐酸除铁锈的反应的方程式是:Fe2O3+6HCl=2FeCl3+3H2O;实验室制取CO2反应物是碳酸钙和盐酸,生成物是氯化钙、水、二氧化碳,用观察法配平,所以方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)反应③是金属与盐反应,可以是铁和硫酸铜反应,生成铜和硫酸亚铁,方程式是:Fe+CuSO4=FeSO4+Cu;因为B是酸,酸与盐反应,可以是碳酸钙与盐酸反应,生成氯化钙、水、二氧化碳,用观察法配平,二氧化碳后面标上上升符号,所以方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)酸、碱、盐之间发生的化学反应都是复分解反应,反应⑤是酸和碱反应生成盐和水,反应的实质是酸电离出来的氢离子与碱电离出来的氢氧根离子结合生成水;
(5)各组离子在水溶液中能大量共存,相互之间结合不能生成沉淀,不能生成气体,不能生成水,A中生成硫酸钡沉淀,不能共存,B中生成水和二氧化碳,不能共存,C中生成水,不能共存,所以D答案正确.
故答案为:(1)氧化物;酸;(2)①;(3)Fe+CuSO4=FeSO4+Cu;CaCO3+2HCl═CaCl2+H2O+CO2↑;(4)复分解;H+、OH-;H2O;(5)D.
分析:盐的化学性质有四个:盐与金属反应、盐与酸反应、盐与碱反应、盐与盐反应.由题目给出的信息可知:“A”物质属于氧化物,“B”物质属于酸,因为金属既能与酸反应又能与盐溶液反应;从物质组成看,一定由三种元素组成的是碱;反应③是金属与盐溶液的反应,铁和硫酸铜溶液反应生成铜和硫酸亚铁,合理即可;反应⑥是酸与盐的反应,可以是碳酸钙与盐酸反应,合理即可;CaCl2溶液与Na2CO3溶液能够反应的实质是:它们在水中解离出的钙离子与碳酸根离子结合成了碳酸钙白色沉淀;在水溶液中能大量共存的是Na+、NO3-,因为它们相互间没有气体、沉淀或水生成,因此能大量共存.
点评:本题考查了盐的化学性质,解决本考点需要根据实验现象综合分析,从而得出正确的结论.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
 构建知识网络是学习和研究化学常用的科学方法.图是小纪同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.
构建知识网络是学习和研究化学常用的科学方法.图是小纪同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应. (2013?和平区模拟)构建知识网络是学习和研究化学常用的科学方法. 右图是小纪同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.请按要求回答下列问题.
(2013?和平区模拟)构建知识网络是学习和研究化学常用的科学方法. 右图是小纪同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.请按要求回答下列问题. 构建知识网络是学习和研究化学常用的科学方法.图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.
构建知识网络是学习和研究化学常用的科学方法.图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.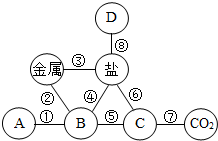 构建知识网络是学习和研究化学常用的科学方法.如图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D表示氧化物、酸、碱、盐的某一种,“-”表示物质之间能够发生化学反应.
构建知识网络是学习和研究化学常用的科学方法.如图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D表示氧化物、酸、碱、盐的某一种,“-”表示物质之间能够发生化学反应.