题目内容
(3分)现有一包含有氯化钠固体的纯碱样品,为测定其成分,同学们取一定质量的这种“纯碱”样品于试管中,加入103g稀盐酸,恰好完全反应,得到4.4g气体。将所得溶液冷却至t℃,恰好成为该温度下的饱和溶液,经测定溶液中的溶质含钠元素的质量为13.8g。求反应后所得溶液中溶质的质量分数。
26.5%
试题分析:解:设碳酸钠的质量为x,生成氯化钠的质量为y。
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
106:x=44:4.4g 117:y=44:4.4g
x =10.6g y =11.7g
设溶质质量为M。
Na ~ NaCl
23 58.5
13.8g m
23:58.5=13.8g:m
m =35.1g
原固体中NaCl的质量为:35.1g—11.7g=23.4g
所得溶液的质量为:23.4g+10.6g+103g—4.4g=132.6g
所得溶液中溶质的质量分数为:(35.1g/132.6g)╳100%≈26.5%
答:反应后所得溶液中溶质的质量分数为26.5%。
点评:根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答;本题的难点在于由钠元素的质量来推算氯化钠的质量。

练习册系列答案
相关题目
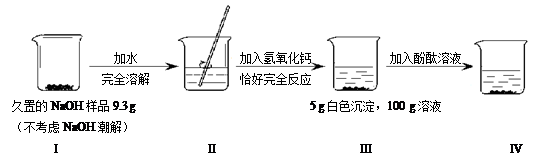
 C(金刚石)+2Na2O。请计算46 g金属钠理论上可制得金刚石的质量。
C(金刚石)+2Na2O。请计算46 g金属钠理论上可制得金刚石的质量。 2NaOH+H2↑+Cl2↑,若生产100 kgNaOH,理论上产生H2多少千克?
2NaOH+H2↑+Cl2↑,若生产100 kgNaOH,理论上产生H2多少千克?