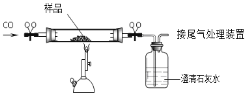
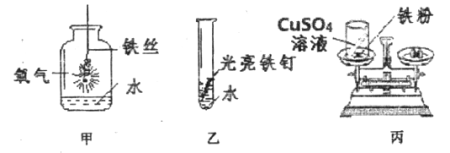
题目内容
【题目】请结合图回答问题:
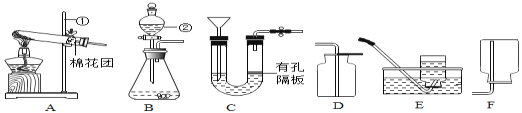
(1)仪器名称:①_________,②__________。
(2)用高锰酸钾制取氧气,可选用的发生装置是_____(选填序号),该反应的化学方程式为_______。用E装置收集氧气完毕后,应先____(选填“a从水中取出导气管”或“b熄灭酒精灯”)。
(3)实验室制取CO2,反应的化学方程式为_________,为方便控制反应的发生和停止,应选择的发生装置是__________(选填序号)。
(4)实验室制备H2 的原料可用__________和稀盐酸,该反应的化学方程式为______。为了控制反应的速度和制得较为纯净的氢气,应选择的发生和收集装置的组合是_____。
【答案】铁架台 分液漏斗 A 2KMnO4![]() K2MnO4+MnO2+O2↑ a CaCO3+2HCl=CaCl2 + CO2↑+ H2O C Zn Zn+2HCl=ZnCl2+H2 ↑ BE(答案合理即可)
K2MnO4+MnO2+O2↑ a CaCO3+2HCl=CaCl2 + CO2↑+ H2O C Zn Zn+2HCl=ZnCl2+H2 ↑ BE(答案合理即可)
【解析】
(1)据图可知仪器①是铁架台;②是分液漏斗;
(2)如果用高锰酸钾制氧气就需要加热,应选择装置A;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;
K2MnO4+MnO2+O2↑;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;C装置能控制反应的发生和停止;
(4)实验室制取氢气的反应物是锌和稀盐酸,反应的化学方程式为:Zn+2HCl==ZnCl2+H2 ↑;反应条件是常温,氢气难溶于水且密度比空气小,具有可燃性和还原性,所以为了控制反应速率和制得较为纯净的氢气,制取氢气应选择的发生装置和收集装置的组合应选择BE。

【题目】分子对应的特性不一致的选项是( )
选项 | 操作或现象 | 分子的特性 |
| 给篮球充气 | 分子间有间隙 |
| 物质热胀冷缩 | 分子大小随温度改变而改变 |
| 在花园中可闻到花的香味 | 分子是运动的 |
| 加热氧化汞可得到金属汞和氧气 | 分子在化学变化中是可以再分的 |
A. A B. B C. C D. D
【题目】我校化学兴趣小组同学为了测定当地石灰石中碳酸钙的质量分数,他们采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(杂质不和盐酸反应,也不溶与水),请帮他们计算:
序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
第1次 | 20 | 11 |
第2次 | 20 | 6 |
第3次 | 20 | 2.8 |
第4次 | 20 | n |
(1)碳酸钙的相对分子质量 _______。
(2)上表中n的数值是 _________ 。
(3)样品中碳酸钙的质量分数 _________ 。
(4)生成二氧化碳的质量为__________(写出计算过程)。
【题目】如图是测定空气中氧气含量的两套实验装置,请据图回答下列问题(提示:铜粉在加热条件下会与氧气反应生成黑色氧化铜固体):
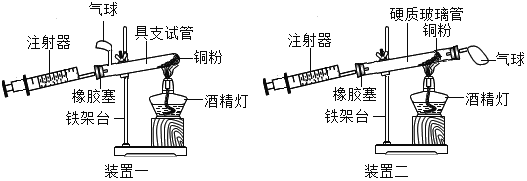
(1)装置一和装置二中气球的位置不同,_____(填“装置一”或“装置二”)更合理,理由是_____.
(2)根据实验测得的相关数据(见下表),计算空气中氧气的体积分数.
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 7mL | _____ |