题目内容
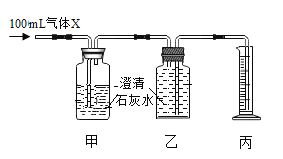
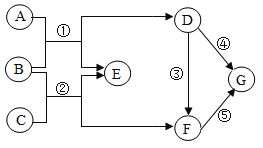
【题目】A~G是初中化学常见的物质,它们之间的转化关系如下图所示。其中A、B、C、E都是氧化物,D、F、G都是金属单质,且G为导电性、导热性最好的金属,A和F均为红色固体(其中部分反应条件、反应物及生成物已略去)。请回答下列问题:
(1)写出A物质的化学式_____;
(2)写出反应②的化学方程式_____;
(3)写出反应④的化学方程式_____;
(4)从微观角度解释B和E两种物质性质不同的原因_____;若将E转化为B,则该反应的化学方程式为_____。
【答案】Fe2O3 ![]()
![]() 分子的构成不同
分子的构成不同 
【解析】
A是氧化物,又是红色的固体,则A是氧化铁;A与氧化物B 反应,生成金属单质D,则D是铁,E是二氧化碳,B是一氧化碳,化学方程式是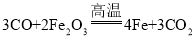 ;B(一氧化碳)与C反应生成红色固体F和E(二氧化碳),则是C氧化铜,F是铜;反应的化学方程式是
;B(一氧化碳)与C反应生成红色固体F和E(二氧化碳),则是C氧化铜,F是铜;反应的化学方程式是![]() ; G为导电性、导热性最好的金属,则G是银,D (铁)与硝酸银反应得到银,化学方程式是
; G为导电性、导热性最好的金属,则G是银,D (铁)与硝酸银反应得到银,化学方程式是![]() ;F(铜)与硝酸银反应也可得到银,反应的化学方程式是
;F(铜)与硝酸银反应也可得到银,反应的化学方程式是![]() 。
。
(1)A物质是氧化铁,它的化学式是Fe2O3;
故填:Fe2O3。
(2)反应②是一氧化碳与氧化铜在加热条件下反应生成铜和二氧化碳,化学方程式是![]() ;
;
故填:![]() 。
。
(3)反应④是铁与硝酸银反应生成银和硝酸亚铁,化学方程式是![]() ;
;
故填:![]() 。
。
(4)B是一氧化碳,E是二氧化碳,二者性质不同的原因是分子的构成不同,将二氧化碳转化为一氧化碳,反应的化学方程式是 ;
;
故填:分子的构成不同  。
。

【题目】下表给出了某些金属的信息。
每吨金属在2018年12月的价格(元) | 地壳中的含量(%) | |
铝 | 13586 | 7.73 |
铂 | 305 000 000 | 0.000 000 1 |
铁 | 4010 | 4.75 |
金 | 339 000 000 | 0.000 000 1 |
(1)依据表中信息解释,金和铂均很昂贵的原因是______。
(2)工业上用含铝、铁的矿石制取铝和铁。
①用赤铁矿炼铁的化学方程式是______。若要得到112t铁,理论上需要Fe2O3的质量为______t。
②将熔融的氧化铝通电分解,可获得铝和另一种单质。反应的化学方程式是______。
③铝抗腐蚀性强的原因是______。