题目内容
【题目】气体制取是重要的化学实验活动,请根据给出如图1装置图回答下列问题: 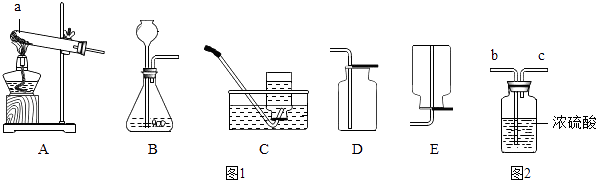
(1)请写出图(1)A中仪器a的名称: .
(2)用高锰酸钾制取并收集较纯的氧气,选择的装置是(填字母序号).
(3)在实验室中选用B装置制取氧气,反应原理是(用化学方程式表示);用这种方法制得的氧气常含有少量水蒸气.若用如图2所示装置除去水蒸气,气体应从(填“b”或“c”)端进入.
(4)实验室制取二氧化碳时,可将放到集气瓶口来判断是否已集满CO2气体,实验室不适宜用排水法收集二氧化碳的理由是 .
【答案】
(1)试管
(2)AC
(3)2H2O2 ![]() 2H2O+O2↑;b
2H2O+O2↑;b
(4)燃着的木条;二氧化碳易溶于水且能与水反应
【解析】解:(1)根据实验室常用仪器可知是试管;(2)实验室用高锰酸钾制取氧气,属于固体加热型,要收集较纯净的氧气要用排水法收集,因此应该选用的装置是AC;(3)过氧化氢在二氧化锰的催化作用下常温即可迅速生成大量氧气,反应原理是:2H2O2 ![]() 2H2O+O2↑;浓硫酸具有吸水性,洗气时长进短出,气体应从b进;(4)二氧化碳验满的方法是用燃着的木条放在集气瓶口,若木条熄灭,证明已满;二氧化碳易溶于水且能与水反应,不适合用排水法收集.答案:(1)试管;(2)AC;(3)2H2O2
2H2O+O2↑;浓硫酸具有吸水性,洗气时长进短出,气体应从b进;(4)二氧化碳验满的方法是用燃着的木条放在集气瓶口,若木条熄灭,证明已满;二氧化碳易溶于水且能与水反应,不适合用排水法收集.答案:(1)试管;(2)AC;(3)2H2O2 ![]() 2H2O+O2↑;b;(4)燃着的木条;二氧化碳易溶于水且能与水反应.
2H2O+O2↑;b;(4)燃着的木条;二氧化碳易溶于水且能与水反应.
【考点精析】关于本题考查的二氧化碳的检验和验满,需要了解验证方法:将制得的气体通入澄清的石灰水,如能浑浊,则是二氧化碳.验满方法:用点燃的木条,放在集气瓶口,木条熄灭.证明已集满二氧化碳气体才能得出正确答案.

【题目】通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐.粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等). [提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
20℃时,一些物质的溶解度 | OH﹣ | CO32﹣ |
Na+ | 溶 | 溶 |
Ca2+ | 微 | 不 |
Mg2+ | 不 | 微 |
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验.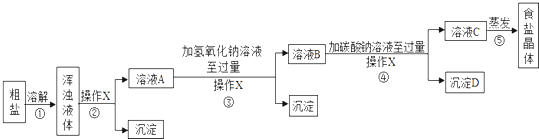
[交流与表达]
(1)实验步骤①和②的目的是;实验步骤③和④的目的是 .
(2)实验操作X的名称是 , 该操作中要用到的玻璃仪器有烧杯、玻璃棒和
(3)实验步骤③的主要目的是(用化学方程式回答);判断氢氧化钠溶液已过量的方法是 .
(4)实验步骤④中生成的沉淀D是 . (填写名称)
(5)实验步骤⑤用蒸发溶剂的方法而不用降低溶液温度的方法获取食盐晶体,原因是;在蒸发食盐溶液的过程中要使用玻璃棒,作用是
(6)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种试剂就能将两种可溶性杂质出去,你认为这种方法(选填“可行”或“不可行”),理由是
(7)有同学认为原实验方案不完善,做出这种评价的依据是 .
(8)为了完善原实验方案,你设计的实验是 . (仅写出补充部分的实验操作和现象)