题目内容
【题目】试管实验节约药品操作简便现象明显,是课堂教学中研究物质性质与变化的重要方法与手段。下列是初中化学中常见的几组实验:
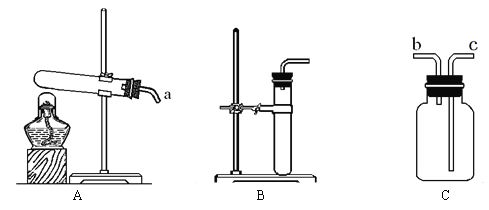
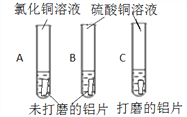
(1)将两片大小、形状相同的未打磨的铝片分别放入A、B两试管中,再分别倒入氯化铜溶液和硫酸铜溶液,结果A试管中产生较多气泡和紫红色固体,B试管中一段时间内无明显现象。将一片单向打磨3次的铝片放入C试管中,加入硫酸铜溶液,打磨处产生一些气泡和紫红色固体。对比AB两试管说明______会影响铝与铜盐溶液的反应。为了验证这一观点,向B试管中加入下列物质中的_______,也产生与A试管同样现象。
A.NaCl溶液 B.Na2SO4溶液 C.KCl溶液 D.稀硫酸
对比BC两试管说明______会影响铝与硫酸铜的反应。
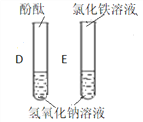
(2)向盛有氢氧化钠溶液的D、E两支试管中分别滴入酚酞试液和氯化铁溶液,D中溶液变红色,E中出现的现象是______,写出E中反应的化学方程式_____。再分别往上述两试管中滴入稀硫酸并充分振荡,能说明试管内恰好完全反应的现象是:D试管中看到______,E试管中看到______,此中和反应有明显现象,请再举一个无需借助指示剂就有明显现象的中和反应实例______(用化学方程式表示)。
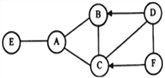
(3)请仔细观察下图:
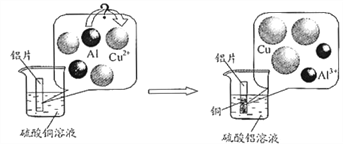
试从微观粒子变化的角度分析该反应的实质是:_________。
【答案】 溶液中的酸根离子(阴离子) AC 铝片表面致密氧化膜 产生红褐色沉淀 3NaOH + FeCl3=Fe(OH)3↓+ 3NaCl 红色刚刚褪为无色 红褐色沉淀消失,溶液呈黄色 H2SO4+Cu(OH)2=CuSO4+2H2O 铝比铜活泼,在溶液中,每2个铝原子失去6个电子,变成2个铝离子;每3个铜离子得到6个电子,变成3个铜原子
【解析】(1)根据对比实验法分析解答;(2)根据氯化铁溶液与氢氧化钠溶液反应生成氢氧化铁红褐色沉淀和氯化钠解答;根据氢氧化钠溶液与硫酸反应生成硫酸钠和水,溶液显中性解答;根据氢氧化铁与硫酸反应生成硫酸铁和水解答;根据中和反应有沉淀生成或消失分析解答。(3)根据微观示意图分析解答。(1)A、B试管中分别装有氯化铜溶液和硫酸铜溶液,其它条件均相同,对比A、B两试管说明溶液中的酸根离子(阴离子)会影响铝与铜盐溶液的反应。A试管中加入的是盐酸盐,故为了产生与A试管同样现象,B试管中也应加入盐酸盐,故选AC;对比BC两试管说明铝片表面致密氧化膜会影响铝与硫酸铜的反应;(2)氯化铁溶液与氢氧化钠溶液反应生成氢氧化铁红褐色沉淀和氯化钠,E中出现的现象是产生红褐色沉淀;反应的化学方程式为3NaOH + FeCl3=Fe(OH)3↓+ 3NaCl;再分别往上述两试管中滴入稀硫酸并充分振荡,能说明试管内恰好完全反应的现象是:D试管中看到红色刚刚褪为无色,E试管中看到红褐色沉淀消失,溶液呈黄色,此中和反应有明显现象。请再举一个无需借助指示剂就有明显现象的中和反应实例:氢氧化铜与硫酸反应生成硫酸铜和水,反应的化学方程式为H2SO4+Cu(OH)2=CuSO4+2H2O。(3)由于金属活动性及微观示意图可知,铝比铜活泼,在溶液中,每2个铝原子失去6个电子,变成2个铝离子;每3个铜离子得到6个电子,变成3个铜原子。

 阅读快车系列答案
阅读快车系列答案【题目】化学兴趣小组的同学一起探究金属的化学性质。
(进行实验)
把打磨后的铁丝放入硫酸铜溶液中,铁丝表面有红色固体析出,得出结论:铁和铜的金属活动性顺序是___________。请写出铁丝放入硫酸铜溶液中的反应方程式____________。
(提出问题)
小组同学验证本实验时出现了异常现象:有的试管中铁丝表面没有红色固体出现,反而出现了黑色固体。为了探究此现象,小组同学进行了以下实验:
实验序号 | ① | ② | ③ |
实验 |
|
|
|
观察时间(分钟) | 3 | 3 | 3 |
生成固体颜色 | 黑色 | 红色 | 红色 |
(解释与结论)
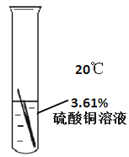
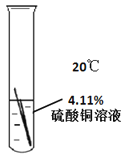
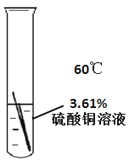
(1)通过上述实验能得出铁丝表面有黑色固体产生,与温度有关的实验序号是_________。
(2)通过上述实验除了能得出铁丝表面有黑色固体产生与温度有关,还能得出与_________有关。
(反思与评价)
针对此异常现象,你还想探究的问题是_________。