题目内容
某化学兴趣小组欲探究铁、铜、锌、银的金属活动性顺序,设计了下图实验(其中金属均已打磨,且其形状、大小相同;所用盐酸的溶质质量分数、用量也相同).
【提出问题】铁、铜、锌、银的金属的活动性由强到弱的顺序是什么?
【猜想与假设】小明同学:锌、铁、铜、银
【实验与探究】小明同学为了验证自己的猜想,进行了以下实验:
【反思与评价】小组同学讨论后认为,以上3个实验不能证明小明同学的猜想,理由是 .
【表达与交流】其中,小天同学提出,只需再补充一个实验即可得出正确的结论.请你帮他补充完整(用化学方程式表示): .
【提出问题】铁、铜、锌、银的金属的活动性由强到弱的顺序是什么?
【猜想与假设】小明同学:锌、铁、铜、银
【实验与探究】小明同学为了验证自己的猜想,进行了以下实验:
| 实验内容 | 实验现象 | 实验结论 |
 |
实验①和实验③的试管中均有气泡产生,但 不同 |
|
| 实验②中观察到: |
铜比银活泼 |
【表达与交流】其中,小天同学提出,只需再补充一个实验即可得出正确的结论.请你帮他补充完整(用化学方程式表示):
考点:金属活动性的探究,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:【实验与探究】(1)从在金属活动顺序表中氢前边的金属可以与稀盐酸反应,且活动性越强反应越剧烈,产生气泡的速率越快去分析解答;
(2)由实验结论:“铜比银活泼”,说明铜可以和硝酸银(无色)反应生成银白色的银和硝酸铜(溶液为蓝色)去分析解答;
【反思与评价】从实验①可以得出:Fe>H,②可以得出:Cu>Ag,③可以得出:Zn>H,综合①③中,锌产生的气泡的速率快可以得出:Zn>Fe;但是无法得出铁和铜的活动性大小去分析解答;
(2)由实验结论:“铜比银活泼”,说明铜可以和硝酸银(无色)反应生成银白色的银和硝酸铜(溶液为蓝色)去分析解答;
【反思与评价】从实验①可以得出:Fe>H,②可以得出:Cu>Ag,③可以得出:Zn>H,综合①③中,锌产生的气泡的速率快可以得出:Zn>Fe;但是无法得出铁和铜的活动性大小去分析解答;
解答:解:【实验与探究】(1)在金属活动顺序表中氢前边的金属可以与稀盐酸反应,且活动性越强反应越剧烈,产生气泡的速率越快;由于金属活动顺序表中,锌的活动性比铁强,所以锌产生氢气的速率大于铁产生氢气的速率;故答案为:产生气泡的速率 锌的活动性大于铁;
(2)由实验结论:“铜比银活泼”,说明铜可以和硝酸银(无色)反应生成银白色的银和硝酸铜(溶液为蓝色);故答案为:铜的表面有银白色固体,且溶液由无色变这蓝色;
【反思与评价】由实验①可以得出:Fe>H,②可以得出:Cu>Ag,③可以得出:Zn>H,综合①③中,锌产生的气泡的速率快可以得出:Zn>Fe;但是无法得出铁和铜的活动性大小;金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以把铁放到硫酸铜溶液中去,铁和硫酸铜反应生成硫酸亚铁和铜,其反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;故答案为:Fe+CuSO4═FeSO4+Cu;
(2)由实验结论:“铜比银活泼”,说明铜可以和硝酸银(无色)反应生成银白色的银和硝酸铜(溶液为蓝色);故答案为:铜的表面有银白色固体,且溶液由无色变这蓝色;
【反思与评价】由实验①可以得出:Fe>H,②可以得出:Cu>Ag,③可以得出:Zn>H,综合①③中,锌产生的气泡的速率快可以得出:Zn>Fe;但是无法得出铁和铜的活动性大小;金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以把铁放到硫酸铜溶液中去,铁和硫酸铜反应生成硫酸亚铁和铜,其反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;故答案为:Fe+CuSO4═FeSO4+Cu;
点评:同学们要会利用金属活动顺序表设计实验,去验证金属的还原性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 2010年5月5日,位于美国墨西哥湾的一个石油钻井平台发生爆炸并引发大火,之后发生漏油,每天多达5000桶以上,引起了国际社会的高度关注,很多国家向美国运送了设备及人员,以帮助美国尽快处理污染问题.7月15日,英国石油公司宣布,新的控油装置已成功罩住水下漏油点.下列说法正确的是( )
2010年5月5日,位于美国墨西哥湾的一个石油钻井平台发生爆炸并引发大火,之后发生漏油,每天多达5000桶以上,引起了国际社会的高度关注,很多国家向美国运送了设备及人员,以帮助美国尽快处理污染问题.7月15日,英国石油公司宣布,新的控油装置已成功罩住水下漏油点.下列说法正确的是( )| A、石油燃烧属于物理变化 |
| B、石油是纯净物 |
| C、此事件已对环境造成严重污染 |
| D、为杜绝环境污染,人类应停止一切石油开采 |
被蚊虫叮咬时分泌的蚊酸(CH2O2)会使人体皮肤肿痛.下列有关蚁酸的说法正确的是( )
| A、蚊酸中含有1个H2分子 |
| B、蚁酸是由碳、氢、氧三种原子构成 |
| C、蚁酸中氢元素质量分数最小 |
| D、蚁酸中碳氧元素的质量比为1:2 |
在一个密闭的容器有甲、乙、丙、丁四种物质,通过电火花引燃后,充分发生反应.经测定,容器内反应前后各物质的质量如图,若甲的相对分子质量为n,丁的相对分子质量为2n,则下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量g | 4 | 10 | 1 | 25 |
| 反应后质量g | 未测 | 21 | 10 | 9 |
| A、该反应一定是置换反应 |
| B、该反应中生成的乙与丙的质量比为11:9 |
| C、甲反应后的质量为4g |
| D、该反应中甲与丁的化学计量数之比为1:2 |
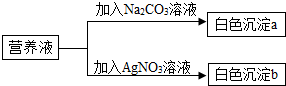 无土栽培是利用营养液栽培作物的一种方法,现有一种无色营养液,可能含有硝酸钙、碳酸钾、氯化钾、硝酸钾中的一种或几种,为探究其成分,某同学设计并完成了如图所示的实验,下列判断正确的是( )
无土栽培是利用营养液栽培作物的一种方法,现有一种无色营养液,可能含有硝酸钙、碳酸钾、氯化钾、硝酸钾中的一种或几种,为探究其成分,某同学设计并完成了如图所示的实验,下列判断正确的是( )| A、营养液中可能含有硝酸钙 |
| B、营养液中一定没有硝酸钾 |
| C、营养液章一定含有碳酸钾 |
| D、营养液中可能由硝酸钙、氯化钾、硝酸钾组成 |
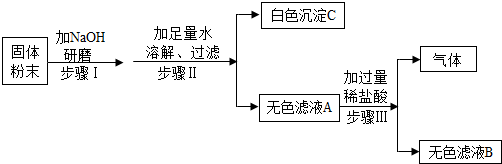
 2013年邵阳市初中毕业和化学实验操作技能考查中,小波抽到的试题是“水的净化”,请你与小波一起试验,并回答下列问题.
2013年邵阳市初中毕业和化学实验操作技能考查中,小波抽到的试题是“水的净化”,请你与小波一起试验,并回答下列问题.