题目内容
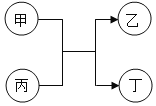
【题目】一种制备氢氧化镁的生产流程如图所示,MgCl2和NaOH按恰好完全反应的比例加料。
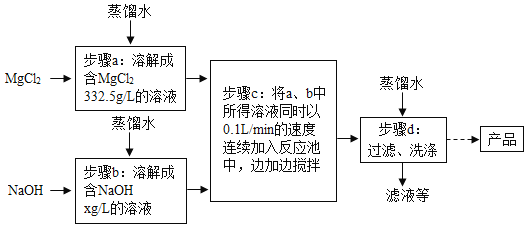
(1)写出步骤c中发生反应的化学方程式:_____。
(2)x=_____。
(3)过滤得到的粗产品还要经过洗涤,洗涤时主要除去的杂质是_____。
(4)如图流程中若用下列物质代替氢氧化钠,也能制得氢氧化镁的是_____。
①盐酸 ②氯化钙 ③氨水 ④硫酸镁
【答案】MgCl2+2NaOH═Mg(OH)2↓+2NaCl 280 氯化钠 ③
【解析】
(1)步骤c中氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,发生反应的化学方程式:MgCl2+2NaOH═Mg(OH)2↓+2NaCl。
故填:MgCl2+2NaOH═Mg(OH)2↓+2NaCl。
(2)根据题意有:
每分钟反应的氯化镁质量:332.5g/L×0.1L=33.25g,
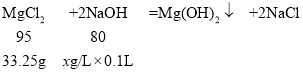
![]() ,解得x=280。
,解得x=280。
故填:280。
(3)过滤得到的粗产品还要经过洗涤,洗涤时主要除去的杂质是反应生成的氯化钠。
故填:氯化钠。
(4)如图流程中若用下列物质代替氢氧化钠,也能制得氢氧化镁的是氨水,是因为氨水是碱,能和氯化镁反应生成氢氧化镁沉淀和氯化铵。
故填:③。

 小题狂做系列答案
小题狂做系列答案【题目】化学课上,老师在一瓶充满CO2软塑料瓶中加入适量NaOH溶液,振荡,发现软塑料瓶变瘪。针对这一有趣的现象,同学们发表自己的见解,请参与其中,并完成下列问题。
(1)小亮同学该现象说明了CO2和NaOH确实发生了反应。塑料瓶变瘪的原因是_____,二者反应的化学方程式为_____。小芳同学提出了质疑,她认为上述实验不足以证明CO2和NaOH确实发生了反应,其原因是_____。
(2)要证明一个反应是否发生,可以从以下两个角度思考。
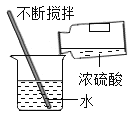
①证实反应物减少。我思考后,设计了如图所示的甲、乙对照实验,该实验需要控制的变量有_____,实验现象是_____。

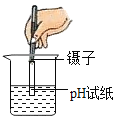
②证实有新物质生成。小霞同学为证明有碳酸钠生成,设计如下实验方案,我们帮她完成。
实验步骤和方法 | 实验现象 | 实验结论 | |
方案一 |
| _____ | CO2和NaOH确实发生了反应 |
方案二 | _____ | _____ |
写出方案二中所涉及的反应化学方程式_____。
(3)由此探究,我得到的启示是_____。(写出一点即可)
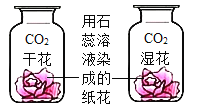
【题目】将冷的浓硫酸加入到装有碳粉的圆底烧瓶中,无明显现象。加热该混合物,有大量气泡产生,现对导出的气体成分进行验证。
[查阅资料]二氧化硫和二氧化碳都能使澄清石灰水变浑浊,其中二氧化硫还能使紫红色的酸性高锰酸钾溶液褪色;无水硫酸铜遇水会由白色变成蓝色。
[提出问题]碳与浓硫酸在加热时,除了生成水和二氧化硫之外,还生成碳的一种氧化物,那么碳的这种氧化物是什么?
[实验猜想]猜想I :CO2 猜想Ⅱ: _________________。
[实验验证]某化学兴趣小组在老师指导下设计了如图实验装置进行验证。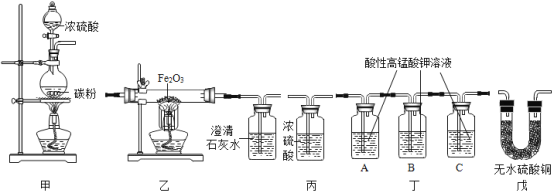
①为了完成对导出气体的验证,请将上述装置进行正确的连接:甲→____→_____→丙→_____(填序号)
②请完成如表中的相关内容:
实验现象 | 实验结论 |
乙中观察到的现象________________ | 猜想I成立 |
丁装置A中溶液褪色 丁装置C中溶液不褪色 | 证明气体中有___________ 装置C的作用_____________ |
戊中白色固体变蓝 | 证明气体中有水蒸气 |
[获得结论]碳与浓硫酸加热反应的化学方程式________________________。