��Ŀ����
����Ŀ���������������벻��������
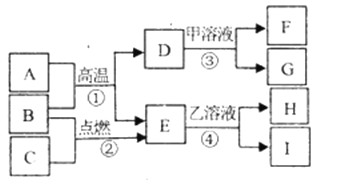
��1��������ɻ�C919����ʹ�úϽ�����ô�������ԭ����ʲô��______��һ�����ɣ�
��2�������ź���ĸ���ǹ�֮������Ϊ��֤�䳤����ˮ�к��в�����ʴ���ɲ�ȡ��Щ��ʩ______����һ�����ɣ�
��3�����������ܶ�С�Ϳ���ʴ�Ժõ��ص��ڸ����Ƚ�ͨ���䷽����;�㷺��
�ٹ�ҵ�ϲ��ø��µ����������������ȡ����д���÷�Ӧ�Ļ�ѧ����ʽ______��
�����ۺ�������������ĩ�Ļ�����ȼ��������������������˷�Ӧ�����ں��Ӹֹ죬д����Ӧ�Ļ�ѧ����ʽ__________���жϷ�Ӧ����Ϊ______��
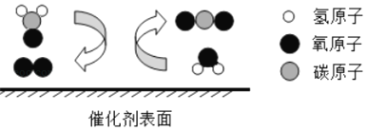
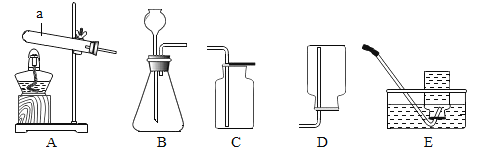
��4����ͼΪʵ����ģ�ҵ��������ԭ�������۲쵽��������______����ʱ����֤���÷�Ӧ�Ѿ�������ֹͣ���ȡ���װ���оƾ��Ƶ�Ŀ����______��
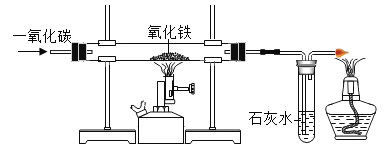
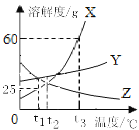
��5��������ʵ�鷴Ӧǰ��ʢʯ��ˮ�Թ��е�����������1.32g�����������ж���g����������ԭ_____��
���𰸡��Ͻ��Ӳ�ȱȴ�������Ӳ�ȴ� Ϳ���� 2Al2O3![]() 4Al+3O2�� 8Al+3Fe3O4
4Al+3O2�� 8Al+3Fe3O4![]() 4Al2O3+9Fe �û���Ӧ ��ɫ����ȫ�����ɫ ��ȼβ������ֹ������һ����̼�ݳ���Ⱦ���� 1.6g
4Al2O3+9Fe �û���Ӧ ��ɫ����ȫ�����ɫ ��ȼβ������ֹ������һ����̼�ݳ���Ⱦ���� 1.6g
��������
��1���Ͻ��Ӳ�ȱȴ�������Ӳ�ȴ���ŵ㣬���Ի�����ʹ�úϽ�����ô�����������Ͻ��Ӳ�ȱȴ�������Ӳ�ȴ�
��2��Ϳ������Ը�������������ˮ�ĽӴ��ﵽ�����Ŀ�ģ����Ϳ���
��3���������з�Ӧ������������������������������������ͨ�磬����ʽΪ��2Al2O3![]() 4Al+3O2�������2Al2O3
4Al+3O2�������2Al2O3![]() 4Al+3O2����
4Al+3O2����
������������������һ��������Ϻ��ڸ����·�Ӧ�����������������÷�Ӧ�����ں��Ӹֹ죬��Ӧ�Ļ�ѧ����ʽ�ǣ�8Al+3Fe3O4![]() 4Al2O3+9Fe���÷�Ӧ���ɵ����뻯���ﷴӦ�����µĵ������µĻ���������û���Ӧ�����8Al+3Fe3O4
4Al2O3+9Fe���÷�Ӧ���ɵ����뻯���ﷴӦ�����µĵ������µĻ���������û���Ӧ�����8Al+3Fe3O4![]() 4Al2O3+9Fe���û���Ӧ��
4Al2O3+9Fe���û���Ӧ��
��4��һ����̼����������Ӧ�������Ͷ�����̼�����Ե��۲쵽��ɫ�����ĩ��Ϊ��ɫ����ʱ����֤���÷�Ӧ�Ѿ�������ֹͣ���ȣ�һ����̼�ж������Ը�װ��ĩ�������Ӿƾ��Ƶ�Ŀ���ǽ�һ����̼ȼ�յ�����ֹ��Ⱦ�����������ɫ����ȫ�����ɫ����ȼβ������ֹ������һ����̼�ݳ���Ⱦ������
��5��������ʵ�鷴Ӧǰ��ʢʯ��ˮ�Թ��е�����������1.32g��Ҳ����������1.32g������̼����������������Ϊx����

![]()
x��1.6g
�𣺲���������1.6g����������ԭ��

����Ŀ������������������������й㷺��Ӧ�á�ʵ��С��ͬѧ�������ϵ�֪�����ᣨH2C2O4����ʹ��������ĸ��������Һ��ɫ������ͬ��������ɫʱ�䲻ͬ������Ӧ�����ʲ�ͬ��С��ͬѧ����������̽����
��������⣩Ӱ��÷�Ӧ��Ӧ���ʵ���������Щ��
���������룩Ӱ��÷�Ӧ��Ӧ���ʵ��������¶ȡ������������Ũ�ȵȡ�
���������ϣ������̣�MnSO4�������÷�Ӧ�Ĵ�����
������ʵ�飩ȡA��B��C��D 4֧�Թܣ�ÿ֧�Թ��зֱ����4mL 0.08% ��KMnO4 ��Һ��0.4 mL �����ᡢ1mL 0.09% �� H2C2O4 ��Һ��

��ʵ���¼��
��� | ��������Ũ�� | �¶� | ���� | ���������ȫ��ɫʱ�� |
A | 98% | ���� | �� | 72s |
B | 65% | ���� | �� | 129s |
C | 65% | 50�� | �� | 16s |
D | 65% | ���� | MnSO4 | 112s |
����������ۣ�
��1������ʹ���������Һ��ɫ��Ӧ�Ļ�ѧ����ʽ���£����ں����ϲ�ȫ����ʽ��
2KMnO4 + 5H2C2O4 + 3H2SO4 == K2SO4 + 2MnSO4 + 10_______+ 8H2O
��2��4֧�Թ�����Ϊ����ʵ�����_______������ţ���ͬ����
��3�����ʵ��A��B��Ŀ���� ______________________________��
��4���Ա�ʵ��B��C�ɵó��Ľ�����_____________________________��
��5��̽�������Ը÷�Ӧ��Ӧ����Ӱ���ʵ����____________________________��
����˼�뽻����
��6��Ӱ��÷�Ӧ��Ӧ���ʵ����س��¶ȡ������������Ũ���⣬��������_______��