题目内容
甲、乙溶解度曲线如图1所示.现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯中,再向烧杯中加入一定量浓硫酸.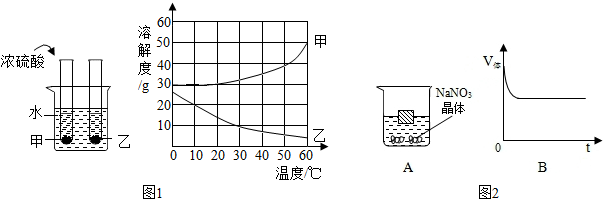
(1)50℃时,甲物质的溶解度是 .
(2)30℃时,甲、乙两种物质的溶解度大小顺序是 .
(3)烧杯中加入浓硫酸后,甲、乙两试管中固体量的变化是 .除了加浓硫酸外,还可以加 物质也会发生这样的变化.
(4)一塑料块飘浮于20℃时的NaNO3饱和溶液中(溶液中有多余NaNO3晶体如图2A所示),当温度改变时(不考虑由此引起的塑料块和溶液体积的变化),塑料块排开液体的体积(V排)随时间(t)发生了如图2B所示的变化.由此推测温度的改变方式是 (填“升温”或“降温”),同时观察到烧杯底部NaNO3晶体 (填“增多”或“减少”).

(1)50℃时,甲物质的溶解度是
(2)30℃时,甲、乙两种物质的溶解度大小顺序是
(3)烧杯中加入浓硫酸后,甲、乙两试管中固体量的变化是
(4)一塑料块飘浮于20℃时的NaNO3饱和溶液中(溶液中有多余NaNO3晶体如图2A所示),当温度改变时(不考虑由此引起的塑料块和溶液体积的变化),塑料块排开液体的体积(V排)随时间(t)发生了如图2B所示的变化.由此推测温度的改变方式是
考点:固体溶解度曲线及其作用,溶解时的吸热或放热现象,晶体和结晶的概念与现象
专题:溶液、浊液与溶解度
分析:(1)根据物质的溶解度曲线可以判断某一温度时物质溶解度的大小;
(2)根据物质的溶解度曲线可以判断某一温度时物质溶解度的大小比较;
(3)浓硫酸、生石灰、氢氧化钠固体等物质溶于水能够放出大量的热;
(4)飘浮的塑料块受到的浮力等于排开液体的重量,当液体密度变大时,排开的液体体积小一些,当液体密度变小时,排开的液体体积大一些.
(2)根据物质的溶解度曲线可以判断某一温度时物质溶解度的大小比较;
(3)浓硫酸、生石灰、氢氧化钠固体等物质溶于水能够放出大量的热;
(4)飘浮的塑料块受到的浮力等于排开液体的重量,当液体密度变大时,排开的液体体积小一些,当液体密度变小时,排开的液体体积大一些.
解答:解:(1)50℃时,甲物质的溶解度是40g.
故填:40g.
(2)30℃时,甲、乙两种物质的溶解度大小顺序是甲>乙.
故填:甲>乙.
(3)烧杯中加入浓硫酸后,温度升高,甲、乙两试管中固体量的变化是甲中的固体减少,乙中的固体增多;
除了加浓硫酸外,还可以加生石灰或氢氧化钠固体物质也会发生这样的变化.
故填:甲中的固体减少,乙中的固体增多;生石灰.
(4)当温度改变时,塑料块排开液体的体积减小,说明液体的密度增大,是因为硝酸钠固体向水中溶解,硝酸钠的溶解度随着温度的升高而增大,因此温度的改变方式升温.
故填:升温;减少.
故填:40g.
(2)30℃时,甲、乙两种物质的溶解度大小顺序是甲>乙.
故填:甲>乙.
(3)烧杯中加入浓硫酸后,温度升高,甲、乙两试管中固体量的变化是甲中的固体减少,乙中的固体增多;
除了加浓硫酸外,还可以加生石灰或氢氧化钠固体物质也会发生这样的变化.
故填:甲中的固体减少,乙中的固体增多;生石灰.
(4)当温度改变时,塑料块排开液体的体积减小,说明液体的密度增大,是因为硝酸钠固体向水中溶解,硝酸钠的溶解度随着温度的升高而增大,因此温度的改变方式升温.
故填:升温;减少.
点评:本题是一道跨学科的题目,解答时要把物理知识和化学知识结合起来进行分析、解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列仪器中,能直接在酒精灯火焰上加热的是( )
| A、烧杯 | B、烧瓶 |
| C、蒸发皿 | D、集气瓶 |
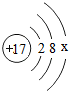 中x=
中x=
 (1)北京奥运村的生活热水都由太阳能热水利用系统提供.下列有关太阳能的说法中,正确的是
(1)北京奥运村的生活热水都由太阳能热水利用系统提供.下列有关太阳能的说法中,正确的是