��Ŀ����
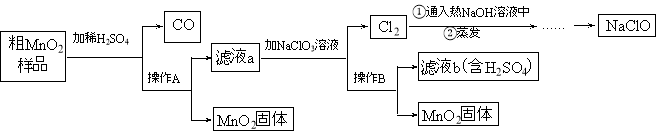
����Ŀ��ij��ѧ��ȤС���θҩ��̼������Ƭ��������̽���������������£�
��ȡһƬθҩ���飬��ˮ��ȫ�ܽ��100g��Һ��
������100g������������0.365%��ϡ����ģ��θ�
��ȡ����20g̼��������Һ������ƿ������εμ�ϡ���ᣬ
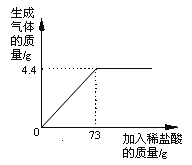
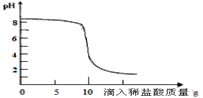
�����ݴ��м��������ҺpH�仯��ͼ��
��ش��������⣺
(1)̼����������___(��������������������������������)��������ϡ��������Ϊ5g�������Һ��___(����������������������)�ԡ�������ϡ��������Ϊ15g�������Һ��������____��
(2)��7.3%��ϡ��������100g������������0.365%��ϡ���ᣬ��Ҫ��ȡ___mL����ˮ��
(3)�����������ƿ�е���10g������������0.365%ϡ����ʱ����������ǡ����ȫ��Ӧ(θҩ�������ɷݲ��μӷ�Ӧ)��������ʵ�����ݼ���ÿƬθҩ��̼�����Ƶ������Ƕ���? ___
���𰸡��� �� �Ȼ��ƺ��Ȼ��� 95 0.42g
��������
����ͼ���Կ���û�м�������ʱ��ҺpH����8��˵��̼��������Һ�Լ��ԣ�������ĵ����������Ϊ10g�Ͷ�Ӧ�Ļ�ѧ����ʽ����ÿƬθҩ��̼�����Ƶ�������
�⣺��1��̼�������������Ӻ�̼��������ӹ��ɵģ������Σ�����ͼ���Կ�����̼��������Һ��pH����8������̼��������Һ�ʼ��ԣ�������ϡ��������Ϊ15g����Һ��pH��7����������������Һ���������Ȼ��ƺ��Ȼ��⣬��7.3%��ϡ���������ˮ������100g ������������0.365%��ϡ���ᣬ��Ҫ����ˮ������Ϊ100g-![]() =95g�ۺ����Ϊ95mL��
=95g�ۺ����Ϊ95mL��
��2�������������20g̼��������Һ�к�̼�����Ƶ�����Ϊx��
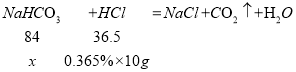
![]()
x=0.084g����һƬθҩ�к��е�̼�����Ƶ�����Ϊ5��0.084g=0.42g��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����̼���ƣ���ѧʽΪ2Na2CO33H2O2����������˫��ˮ������ˮ�ɿ�����Na2CO3��Һ��H2O2��Һ��ϡ�Ϊ�˷��㱣�棬��̼������Ʒ��������������MgSO4����þ�е�һ�ֻ������Ϊ�ȶ�������֪��˫��ˮ�����ڹ�����������Ư�ף��ڹ���þ������ˮ��
��1����̼���Ƶ���;����������____��
A ��ع����� B ������ C ����� D Ư��
��2��������̼�������м�����������ʱ�����ᵼ������̼����������___������ţ���
A �������� B ϡ���� C ������ D ʯ��ˮ
��3��ȡ������̼������Ʒ���ձ��У�������������ˮ���в�����ˮ�Ĺ���������ж���Ʒ��__�й���þ������д������������һ������
��4������ʵ������ѡ�Լ������ʵ��ȷ������Ʒ���Ƿ�����������MgSO4��
��ѡ�Լ���ϡ���ᡢϡH2SO4��BaCl2��Һ������ˮ��AgNO3��Һ
ʵ����� | Ԥ������ͱ�Ҫ���� |
����1��ȡ������Ʒ���ձ��У�����������������ˮ����ֽ��裬���ã����ˡ� |
|
����2��ȡ��������1���õ���Һ���Թ��У�����_______�����á� | _______�� |
����3��ȡ��������2���õ���ҺҺ���Թ��У�_______________�� | ____��˵����Ʒ����MgSO4�� ___��˵����Ʒ��û��MgSO4�� |
˼��������2�У��Ӹ��Լ���Ŀ���ǣ�_____��
����Ŀ��ijѧϰС���̼���ơ�̼�����ƺ�ϡ����ķ�Ӧ������̽����
��1���ֱ���ʢ������̼���ƣ��׳�_________����̼�����ƹ�����Թ��м���������ϡ���ᣬ�۲쵽�����ҷ�Ӧ�Ҳ����������ݡ�̼�����ƺ�ϡ���ᷴӦ�Ļ�ѧ����ʽΪ________
��������⣩
̼���ơ�̼�����ƺ�ϡ���ᷴӦ����������̼�Ŀ����Ƿ���ͬ��
�������ʵ�飩
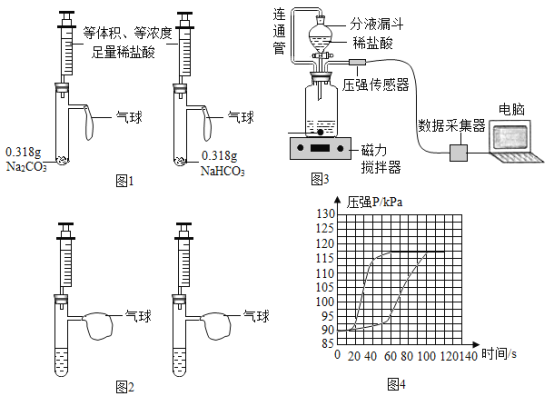
��2������Ƶ�ʵ����ͼ1��ʾ��ʵ��ʱ����ע�����е�ϡ����Ӧ_________������������۲쵽ͼ2��ʾ�����������ó�̼�����ƺ�ϡ���ᷴӦ����������̼�Ͽ�Ľ��ۡ�
��3���ҶԼ�ʵ����������ɣ���̼���ơ�̼�����ƹ����ϡ���ᷴӦ���ܾ��ң�ͨ���۲�����жϲ�������Ŀ�������___________������Ϊ��Ӧȡ��̼Ԫ��������ͬ��̼���ƺ�̼�����ƣ���̼���Ƶ�������Ϊ0.318g��Ӧ��ȡ________ g̼�����ơ�
��4��С��ͬѧ����ʦָ���������ͼ3��ʾ��ʵ�顣
����ͨ�ܵ�������________
�ڷֱ�ȡ���������̼Ԫ��������ͬ��̼���ơ�̼������ϡ��Һ����2�η�̪��Һ�����Լ���ͬ�������ͬŨ�ȵ�������ϡ�������ʵ�顣ʵ��ʱ����Һ��ɫ�仯��¼���1�����ƿ��ѹǿ��ʱ��仯��ͼ4��ʾ��
�����̪��Һ | ����ϡ���ᣬ��Һ��ɫ�仯 | |
̼������Һ | ��ɫ | ��ɫ��dz��ɫ����ɫ |
̼��������Һ | dz��ɫ | dz��ɫ����ɫ |
��ʵ����ۣ�
��5������ͼ4��ʾ��ʵ�����ݿɵõ��Ľ����ǣ���ͬ�����£�____________��ϡ���ᷴӦ����������̼�ϡ��죬������__________
����˼��Ӧ�ã�
��6��С��ͬѧ������1ʵ�������ͼ4���ݣ��ó���һ�����ʺ�ϡ���ᷴӦ����������̼������ԭ���ǣ�____________�����ñ�Ҫ�����ֺͻ�ѧ����ʽ˵������
��7��ͨ������̽���������С��ͬѧ�����ֻ���Թܺͽ�ͷ�ιܼ���̼������Һ��ϡ�����ʵ�顣
���� | ����ͽ��� |
δ֪��Һ�ֱ���Ϊa��b��ȡ����a��Һ���Թ��У��ý�ͷ�ι���ε���b���� | __________ |