题目内容
【题目】水是一种重要的资源。
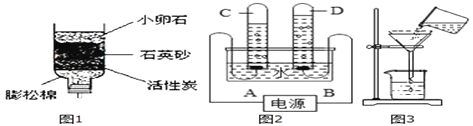
Ⅰ. 为验证水的组成,兴趣小组用图示装置(夹持仪器省略)进行实验。
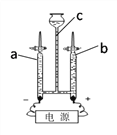
(1)电解时能观察到的现象有_____________(填字母)。
A.连接电源两端的电极上均有气泡产生
B.管a与管b中液面下降
C.管a与管b中产生的气体体积比约为1︰2
D.管c中液面上升
(2)一段时间后关闭电源,用燃着的木条置于b管尖嘴口处,打开活塞,能观察到_________。
(3)该实验说明水是由 ____________组成的。请写出电解水的化学方程式____________。保持水的化学性质的最小粒子是___(写名称)。
Ⅱ.自来水厂净水过程如图所示:
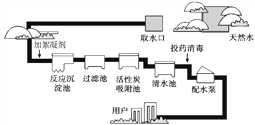
(1)下列说法正确的是_______(填字母)。
A.过滤池可以除去难溶性杂质
B.活性炭吸附池可以将硬水软化
C.清水池中的水是纯净物
D. 可用肥皂水区分硬水和软水
(2)明矾能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。写出氢氧化铝的化学式为__________。
(3)高铁酸钾[K2FeO4]是多功能水处理剂,K2FeO4中铁元素的化合价为________。与水反应的化学方程式为4K2FeO4+10H2O = 4Fe(OH)3↓+8X+3O2↑,则X为______。
A.K2O B.KOH C.K D.KH
【答案】 ABD 木条燃烧更旺 氢元素和氧元素 2H2O![]() 2H2↑+ O2↑ 水分子 AD Al(OH)3 +6 B
2H2↑+ O2↑ 水分子 AD Al(OH)3 +6 B
【解析】Ⅰ. (1)根据电解水的实验现象解答;
(2)根据氧气有助燃性解答;
(3)根据水由氢元素和氧元素组成且水在通电的条件下分解生成氢气和氧气解答;根据由分子构成的物质分子是保持其化学性质的最小粒子解答;
Ⅱ(1) A.根据过滤适用于分离不溶于水的固体和液体分析;
B.根据活性炭具有吸附性分析;
C.根据自然界中的水都是混合物分析;
D.根据硬水和软水的鉴别分析;
(2)根据氢氧化铝中铝元素的化合价为+3价,氢氧根离子的化合价为-1价写出化学式;
(3)根据化合物中各元素正负化合价代数和为0及质量守恒定律分析解答。
解:Ⅰ. (1) A.通电后,连接电源两端的电极上均有气泡产生,正确;
B. 通电后,连接电源两端的电极上均有气泡产生,生成的气体都聚集试管的上方。在气压的作用下,管a与管b中液面下降,正确;
C.管a连接的是电源的负极,管b连接的是电源的正极,电解水实验中正负极产生的气体体积比约为1︰2,故错误;
D.在气压的作用下,将管a与管b中的水压入到管c中,故管c中液面上升,正确。
故选ABD。
(2) 管b连接的是电源的正极,生成的气体是氧气。一段时间后关闭电源,用燃着的木条置于b管尖嘴口处,打开活塞,能观察到:木条燃烧更旺;
(3)该实验说明水是由氢元素和氧元素组成的。电解水的化学方程式为:2H2O 通电 2H2↑+ O2↑。水是由水分子构成的,故保持水的化学性质的最小粒子是:水分子;
Ⅱ(1) A.过滤池可以除去难溶性杂质,正确;
B.活性炭有吸附性,可除去水中的色素及异味,但不能将硬水软化,故错误;
C.清水池中的水是混合物,故错误;
D. 硬水中滴加肥皂水的现象是浮渣多,泡沫少,软水中滴加肥皂水的现象是泡沫多,浮渣少,故可用肥皂水区分硬水和软水,正确。
故选AD。
(2)氢氧化铝中铝元素的化合价为+3价,氢氧根离子的化合价为-1价,故氢氧化铝的化学式为:Al(OH)3 ;
(3)在高铁酸钾中,钾元素的化合价是+1,氧元素的化合价是-2,设铁的化合价是x,
则有(+1)×2+(-2)×4+x=0,可以求出铁元素的化合价为+6;
根据质量守恒定律化学反应前后原子的种类和数目不变,反应前K:8 ,Fe:4 ,O:26,H:20。反应后Fe:4 ,O:18,H:12,X前有系数8,故要除以8,那么X的化学式为KOH。