题目内容
【题目】呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂。为了探究其反应原理,兴趣小组同学在老师的指导下,进行了如下探究。
[查阅资料]过氧化钠在常温下与水、二氧化碳反应分别生成氢氧化钠、碳酸钠和氧气。
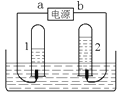
[设计实验]小南同学想通过如图所示装置探究过氧化钠与二氧化碳的反应,并验证反应产物。

(1)C中氢氧化钠的作用是______。
(2)通过上述实验,明明同学认为Na2O2与CO2反应除了生成Na2CO3和O2,还有可能生成NaHCO3.你认为他的结论正确吗?理由是______。写出Na2O2与二氧化碳反应的化学方程式______。
(3)请说说呼吸面具或潜水艇用过氧化钠作为供氧剂的最大的是优点______。
【答案】除去氧气中的二氧化碳 不正确,因为化学反应前后元素种类不变,反应前没有氢元素 2Na2O2+2CO2=2Na2CO3+O2 操作简便,无污染
【解析】
(1)过氧化钠和二氧化碳反应过程中肯定有没反应的二氧化碳混合在氧气中出来,氢氧化钠能与二氧化碳反应生成碳酸钙钠和水,能吸收二氧化碳。为了收集到纯的氧气,可以用氢氧化钠除去氧气中的二氧化碳。
(2)过氧化钠和二氧化碳反应不可能生成碳酸氢钠,因为在反应前没有氢元素,而化学反应前后元素种类不变的;过氧化钠和二氧化碳反应生成碳酸钠和氧气,化学方程方程式为:2Na2O2+2CO2=2Na2CO3+O2;
(3)呼吸面具或潜水艇用过氧化钠作为供氧剂的最大的优点是操作简便,无污染。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目