题目内容
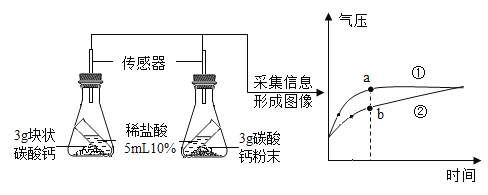
【题目】在密闭容器内有氧气、二氧化碳、水蒸气和一种未知物质W,在一定条件下充分反应,相关内容如下图所示。
反应前后各物质的质量:
物质 | 氧气 | 二氧化碳 | 水蒸气 | W |
反应前质量/g | 50 | 1 | 1 | 23 |
反应后质量/g | 2 | 45 | 28 | x |
反应的微观示意图:

(1)X=_____。
(2)一个C物质分子由_____构成。
(3)反应过程中B物质与D物质的分子个数比为_____。
(4)W的化学式为_____。
【答案】0 1个碳原子和2个氧原子 1:1 ![]()
【解析】
(1)由题意根据质量守恒定律,x=(50g+1g+1g+23g)-(2g+45g+28g)=0。
(2)由微观示意图可知,C是二氧化碳分子,一个二氧化碳分子由1个碳原子和2个氧原子构成。
(3)由表格中的数据可知,参加反应的B氧气和D水的质量比为48g: 27g=16:9,设反应过程中物质B与D物质的分子个数分别为x、y,结合反应有![]() ,解得x:y=1:1。
,解得x:y=1:1。
(4)根据质量守恒定律定律,W中一定含有碳元素和氢元素,二氧化碳中氧元素的质量为![]() ,水中氧元素的质量为
,水中氧元素的质量为![]() ,二氧化碳和水中氧元素的总质量为32g+24g=56g,大于参加反应的氧气的质量48g,即W中含有氧元素,质量为56g-48g=8g,根据质量守恒定律元素守恒,W中碳元素的质量为
,二氧化碳和水中氧元素的总质量为32g+24g=56g,大于参加反应的氧气的质量48g,即W中含有氧元素,质量为56g-48g=8g,根据质量守恒定律元素守恒,W中碳元素的质量为![]() ,W中氢元素的质量为23g-12g-8g=3g,则W中C、H、O三种原子的个数比为
,W中氢元素的质量为23g-12g-8g=3g,则W中C、H、O三种原子的个数比为![]() ,因此W的化学式为
,因此W的化学式为![]() 。
。

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目