题目内容
【题目】化学实验可以帮助我们更好地了解物质的性质和化学原理。根据下列实验装置或实验操作回答问题。
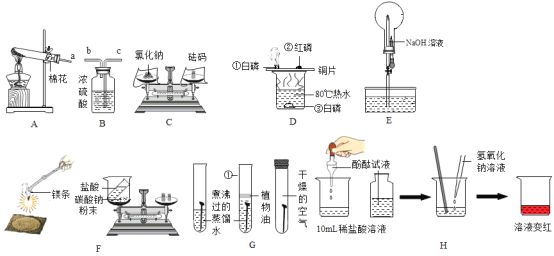
(1)图A中铁制仪器的名称是_____。用装置A制取氧气的化学方程式是_____,用图B干燥O2,气体应从_____(填“b”或“c”)口进入。
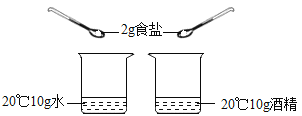
(2)配制一定溶质质量分数的氯化钠溶液,图C的操作称量氯化钠时,称量完毕发现砝码生锈严重,若其他操作均正确,则配制的氯化钠溶液的浓度会_____(填“偏大”、“偏小”或“无影响”)。
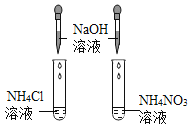
(3)如图D所示,由①处的白磷燃烧,②处的红磷不能燃烧的现象,说明可燃物燃烧需满足的条件是_____。
(4)用图E装置可制造十分有趣的“化学喷泉”现象,将胶头滴管中的NaOH溶液挤进圆底烧瓶时,很快看到长导管顶端产生“喷泉”现象,若将烧瓶内的CO2换成下列四种气体中的_____(填序号)仍可产生“喷泉”现象。
A H2B SO2C CO D HCl
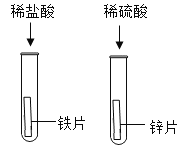
(5)F图中的两种装置都无法用于验证质量守恒定律,若还需用这两个化学反应来验证则该装置改进的方法是_____。
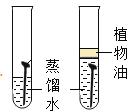
(6)G图是铁生锈条件的探究,其中试管①中用煮沸过的蒸馏水浸泡铁钉的目的是_____。
(7)H图是小丽同学在验证氢氧化钠与稀盐酸能否反应的实验时,错把酚酞溶液滴入稀盐酸中,开始加入氢氧化钠时无明显现象,继续加入氢氧化钠发现溶液变成红色,此实验也能证明盐酸和氢氧化钠反应;当溶液变红时,溶液中的溶质有_____(填化学式)。
【答案】铁架台 ![]() c 偏大 温度达到可燃物的着火点 BD 在密闭容器中进行 除去溶于水的氧气 NaCl、NaOH
c 偏大 温度达到可燃物的着火点 BD 在密闭容器中进行 除去溶于水的氧气 NaCl、NaOH
【解析】
(1)图A中铁制仪器的名称:铁架台。因为装置A中有棉花,所以其中发生的反应是高锰酸钾加热产生锰酸钾、二氧化锰和氧气,化学方程式是![]() ,用图B浓硫酸干燥O2,气体应“长管进、短管出”从c口进入,进行干燥。
,用图B浓硫酸干燥O2,气体应“长管进、短管出”从c口进入,进行干燥。
(2)配制一定溶质质量分数的氯化钠溶液,图C的操作称量氯化钠时,称量完毕发现砝码生锈严重,则右盘质量偏大,若其他操作均正确,则左盘氯化钠质量偏大,配制的氯化钠溶液的浓度会偏大。
(3)①处的白磷燃烧,②处的红磷不能燃烧的现象,但都与空气接触,说明可燃物燃烧需满足的条件是:温度达到可燃物的着火点才可以燃烧;
(4)将胶头滴管中的NaOH溶液挤进圆底烧瓶时,很快看到长导管顶端产生“喷泉”现象,是因为氢氧化钠和二氧化碳反应,使瓶内压强减小,产生“喷泉”现象。如果某气体能和氢氧化钠溶液反应或易溶于水使瓶内压强减小,CO2就可换成该气体,仍可产生“喷泉”现象。
A、H2 不能溶于水,装置内压强基本不变,不能产生喷泉现象;
B、SO2 能与氢氧化钠反应,装置内压强变小,能产生喷泉现象;
C、CO不能溶于水,装置内压强基本不变,不能产生喷泉现象;
D、HCl能与氢氧化钠反应,装置内压强变小,能产生喷泉现象;
故选BD。
(5)F图中的两种装置中有气体参加反应,或有气体生成都无法用于验证质量守恒定律,若还需用这两个化学反应来验证则该装置改进的方法是:在密闭容器中进行;
(6)G图是铁生锈条件的探究,其中试管①中用煮沸过的蒸馏水浸泡铁钉的目的是:除去溶于水的氧气,防止干扰实验;
(7)H图是小丽同学在验证氢氧化钠与稀盐酸能否反应的实验时,错把酚酞溶液滴入稀盐酸中,开始加入氢氧化钠时无明显现象,继续加入氢氧化钠发现溶液变成红色,此实验也能证明盐酸和氢氧化钠反应产生氯化钠;当溶液变红时,说明氢氧化钠过量,溶液中的溶质有:氯化钠(NaCl)和氢氧化钠(NaOH )。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】工业上用纯碱和石灰石为原料制备烧碱的简要工艺流程如下图所示
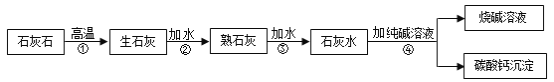
(1)石灰石、生石灰、熟石灰均能与下列___________(填字母)发生化学反应。
A水 B.盐酸 C二氧化碳 D草木灰
(2)写出上述工艺流程中第四步的化学反应方程式______________。
(3)某研究性学习小组的同学想检验上述工艺中的烧碱溶液里是否含有纯碱,甲同学选择了一种酸溶液,乙同学选择了一种碱溶液,丙同学选择了一种盐溶液,他们都能达到检验目的。请在下表中写出甲乙丙所用物质的化学式
甲 | 乙 | 丙 |
______ | _______ | _________ |
(4)步骤④中检验碳酸钙沉淀已洗涤干净的方法是_____________。
【题目】在密闭容器内有氧气、二氧化碳、水蒸气和一种未知物质W,在一定条件下充分反应,相关内容如下图所示。
反应前后各物质的质量:
物质 | 氧气 | 二氧化碳 | 水蒸气 | W |
反应前质量/g | 50 | 1 | 1 | 23 |
反应后质量/g | 2 | 45 | 28 | x |
反应的微观示意图:

(1)X=_____。
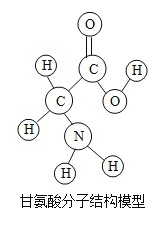
(2)一个C物质分子由_____构成。
(3)反应过程中B物质与D物质的分子个数比为_____。
(4)W的化学式为_____。