题目内容
【题目】氧气、二氧化碳是我们身边常见的物质。某兴趣小组对这两种气体研究如下:
Ⅰ.氧气、二氧化碳的制备:

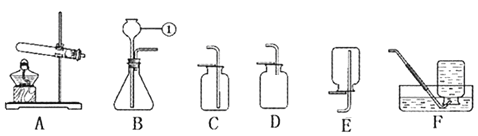
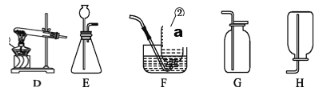
(1)写出A图中有标号仪器的名称:①________。
(2)写出用KMnO4制取O2的化学反应符号或文字表达式________________________。该装置中棉花团的作用是___________________,图中装置一处明显的错误是_____________________。
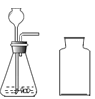
(3)在化学实验室中用石灰石和稀盐酸来制取二氧化碳可选用图B所示的发生装置,该反应的符号或文字表达式是______________,该装置检查气密性的方法是___________。
(4)制二氧化碳也可选用如图C所示的装置,装置中多孔隔板的作用是_______________________;用图D所示的装置也可以制取二氧化碳,将石灰石放在铜丝网中,该实验说明了铜________(填“能”或“不能”)和稀盐酸发生反应。
Ⅱ.氧气的收集及二氧化碳的性质研究:
(1)二氧化碳的性质研究
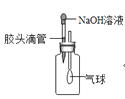
①如图E所示的装置可以测定一段时间收集的二氧化碳的体积,植物油的作用是______________。
②如图F所示的装置说明了二氧化碳具有________________________的性质,该性质在实际生活中的应用是____________。
③已知:CO2和SO2既有相似性,又有差异性。

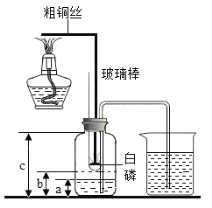
实验一:将收集满两种气体的试管同时倒立于盛水的水槽中,片刻后实验现象如右图所示,说明相同条件下SO2比CO2______(填“易”或“难”)溶于水。
实验二:已知镁条可以在CO2中剧列燃烧: Mg+CO2![]() MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧,__________________。
MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧,__________________。
(2)氧气的收集
(实验1)用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
(实验2)用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
(实验3)用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1 | 实验2 | 实验3 | ||||||||
氧气的体积分数(%) | 79.7 | 79.6 | 79.9 | 88.4 | 89.0 | 87.9 | 90.0 | 89.8 | 89.3 | |
氧气的平均体积分数(%) | 79.7 | 88.4 | 89.7 | |||||||
数据
①由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是_____________。
②不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是_____________。
【答案】酒精灯高锰酸钾![]() 锰酸钾+二氧化锰+氧气或KMnO4
锰酸钾+二氧化锰+氧气或KMnO4![]() K2MnO4+MnO2+O2防止高锰酸钾粉末进入导管 试管口朝上 碳酸钙+盐酸→氯化钙+水+二氧化碳或CaCO3+HCl→CaCl2+H2O+CO2用止水夹夹住右侧 胶皮管,向长颈漏斗内加水,一段时间后漏斗中形成稳定的水柱 控制反应的停止和发生 不能 防止二氧化碳溶于水、和水反应 不支持燃烧且密度比空气大 灭火 易 生成白色和淡黄色固体,放热 验满后继续收集一段时间 水蒸气留存在集气瓶中
K2MnO4+MnO2+O2防止高锰酸钾粉末进入导管 试管口朝上 碳酸钙+盐酸→氯化钙+水+二氧化碳或CaCO3+HCl→CaCl2+H2O+CO2用止水夹夹住右侧 胶皮管,向长颈漏斗内加水,一段时间后漏斗中形成稳定的水柱 控制反应的停止和发生 不能 防止二氧化碳溶于水、和水反应 不支持燃烧且密度比空气大 灭火 易 生成白色和淡黄色固体,放热 验满后继续收集一段时间 水蒸气留存在集气瓶中
【解析】
Ⅰ.(1)图中有标号仪器的名称:①是酒精灯;
(2)在加热的条件下,高锰酸钾生成锰酸钾、二氧化锰和氧气,反应符号或文字表达式:高锰酸钾![]() 锰酸钾+二氧化锰+氧气或KMnO4
锰酸钾+二氧化锰+氧气或KMnO4![]() K2MnO4+MnO2+O2;试管口要放一团棉花,以防止高锰酸钾粉末进入导管;给固体加热时,试管口要略向下倾斜,以防冷凝水回流使试管炸裂;
K2MnO4+MnO2+O2;试管口要放一团棉花,以防止高锰酸钾粉末进入导管;给固体加热时,试管口要略向下倾斜,以防冷凝水回流使试管炸裂;
(3)用石灰石和稀盐酸来制取二氧化碳的符号或文字表达式是:碳酸钙+盐酸→氯化钙+水+二氧化碳或CaCO3+HCl→CaCl2+H2O+CO2;该装置检查气密性的方法是用止水夹夹住右侧胶皮管,向长颈漏斗内加水,一段时间后漏斗中形成稳定的水柱,证明装置不漏气;
(4)制二氧化碳也可选用如图C所示的装置,装置中多孔隔板的作用是可以随时控制反应;用图D所示的装置也可以制取二氧化碳,将石灰石放在铜丝网中,该实验说明了铜不能和稀盐酸发生反应;
Ⅱ.(1)①如图E所示的装置可以测定一段时间收集的二氧化碳的体积,二氧化碳能溶于水,所以加入少量的植物油;
②图F所示的装置说明了二氧化碳具有二氧化碳既不能燃烧、也不能支持燃烧,密度比空气大的性质;二氧化碳可用来灭火;
③实验一:根据图示可以看出,二氧化硫的这支试管内液面上升的明显,故二氧化硫的溶解性强于二氧化碳;
实验二:根据二氧化碳与镁的反应可以推知镁在二氧化硫中燃烧生成氧化镁和硫,同时放出大量的热,氧化镁是白色的,硫是黄色的,故会观察到产生白色和黄色固体;
(2)①根据实验1、2的操作可知,实验2延长了氧气收集的时间,从而使瓶中氧气的体积分数有所提升,所以如果想提高获得的氧气体积分数,可以采取延长收集时间的措施;
②如果各项操作没有问题,实验3获得的氧气体积分数不能达到100%的主要原因可能是用排水法收集会形成水蒸气留存在集气瓶中。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
(提出猜想)除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
(完成实验)按下表进行测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
(分析数据、得出结论)
(1)由实验__________与实验④对比,证明猜想合理。
(2)实验所用的三种物质,催化效果最好的是_________________。
(反思)
(3)若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后______________不变;
(4)氯酸钾能被氧化铁催化分解放出氧气的文字表达式为____________ 。