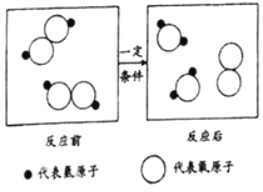
题目内容
【题目】某实验活动小组的同学要提纯含有CaCl2、Na2SO4及泥沙等杂质的粗盐,先将粗盐溶于适量水中,再按以下流程进行处理:
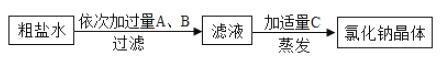
(1)试剂B是_____(从碳酸钠溶液、碳酸钾溶液、氢氧化钡溶液、硝酸钡溶液中选择)。
(2)写出一个加入A时发生反应的化学方程式_____。
(3)加适量C的目的是什么_____?
【答案】碳酸钠溶液 Na2SO4+Ba(OH)2═BaSO4↓+2NaOH 除去过量的碳酸根离子和氢氧根离子
【解析】
根据硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸盐要放在加钡盐溶液之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子,进行分析解答。
(1)硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氢氧化钡溶液溶液之后,这样碳酸钠会除去反应剩余的氢氧化钡溶液。不能选用硝酸钡溶液,否则会引入新杂质硝酸钠。
(2)加入的试剂A是氢氧化钡溶液,即硫酸钠与氢氧化钡反应生成硫酸钡白色沉淀和氢氧化钠,方程式为Na2SO4+Ba(OH)2═BaSO4↓+2NaOH。
(3)滤液中含有氢氧根离子和碳酸根离子,加适量C,目的是除去过量的碳酸根离子和氢氧根离子。

 走进文言文系列答案
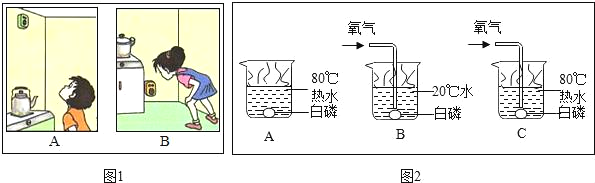
走进文言文系列答案【题目】有A、B两瓶未知无色液体,分别是碳酸钠溶液和氢氧化钡溶液,为鉴别出两种无色液体,同学们设计了如图所示甲、乙、丙三种实验方案。
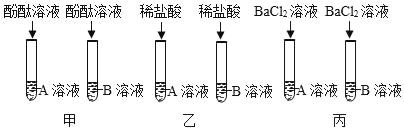
(1)甲、乙、丙三种方案中,不可行的是_____,原因是_____。
(2)请写出丙方案中发生反应的化学方程式_____。
(3)小红同学把丙方案反应后的废液倒入一个洁净的烧杯中,过滤,得白色沉淀和无色滤液,同学们对滤液成分进行了进一步的探究。
(提出问题)滤液中除了Na+,还含有什么离子?
(作出猜想)
猜想一:含有OH﹣、Cl﹣、CO32﹣
猜想二:含有OH﹣、C1﹣、Ba2+
猜想三:含有_____(填离子符号)
(实验探究)
实验操作 | 实验现象 | 结论 |
取少量滤液于试管中,向其中滴加少量的硫酸钠溶液 | 无明显现象 | 猜想一正确 |
(评价交流)
①你认为同学们的结论_____(填“正确”或“不正确”),理由是_____。
②同学们经过讨论后一致认为:若将硫酸钠溶液换成足量的_____,就能确定滤液中的离子成分。
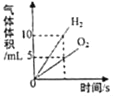
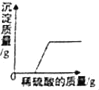
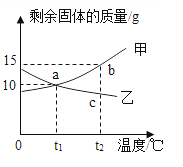
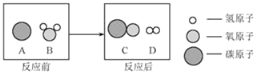
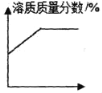
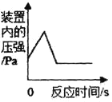
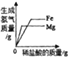
【题目】下列4个坐标图分别示意实验过程中某些量的变化,其中正确的是( )
A | B | C | D |
浓硫酸敝口放置一段时间 | 在某一密闭装置内点燃红磷 | 向一定质量的二氧化锰中加入过氧化氢溶液 | 向等质量的铁、镁中 滴加稀盐酸 |
|
|
|
|
A. AB. BC. CD. D