题目内容
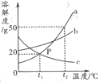
【题目】甲、乙两种物质的溶解度曲线如图所示,下列说法不正确的是
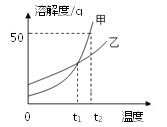
A. t2℃时,甲的溶解度大于乙的溶解度
B. t2℃时,甲的饱和溶液中溶质与溶剂的质量比为1∶2
C. t1℃时,甲、乙两种溶液的溶质质量分数相等
D. t2℃时,相同质量的甲、乙饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙
【答案】C
【解析】A. 在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。t2℃时,甲的溶解度大于乙的溶解度,正确;B. 溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。t2℃时,甲的溶解度为50g,饱和溶液中溶质与溶剂的质量比为1∶2,正确;C. ![]() ,t1℃时,甲、乙两种物质的溶解度相同,其饱和溶液的溶质质量分数相等,错误;D. t2℃时,甲的溶解度比乙的大,相同质量的甲、乙饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙,正确。故选C。
,t1℃时,甲、乙两种物质的溶解度相同,其饱和溶液的溶质质量分数相等,错误;D. t2℃时,甲的溶解度比乙的大,相同质量的甲、乙饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙,正确。故选C。

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
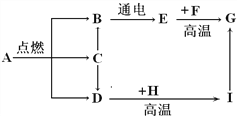
ABC考王全优卷系列答案【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
查阅资料
a.固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。
b.氯化钙、氯化溶液均呈中性。
(提出问题)
①酒精中是否含有碳元素?
②固体酒精中的氢氧化钠是否变质?
(实验探究)
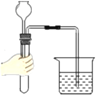
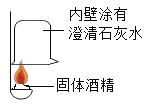
①按右图所示进行实验,发现烧杯内壁有一层白膜,可得出酒精中含有碳元素的结论,理由是_______________。
②取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀是如何形成的:_______________由此说明氢氧化钠已变质。
③为进一步确定氢氧化钠的变质程度,分组进行探究。
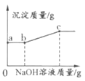
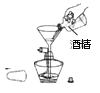
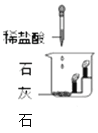
甲组同学取烧杯上层清液于两支试管中,按下图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生______________ |
实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是_______________
他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)乙组实验中加足量氯化钡溶液的目的是_____________
(实验结论]小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。
【题目】某实验小组在做“用澄清石灰水检验二氧化碳”的实验时,发现一个有趣的实验现象:
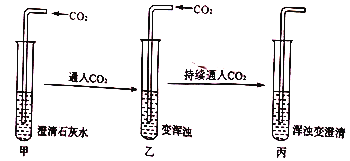
试管中浑浊现象为何消失?实验小组的同学对此实验进行了下列探究活动:
(1)根据已学知识,实验小组对CO2使澄清石灰水变浑浊的现象作出了合理的解释,其化学方程式为____________________。
(2)(查阅资料)
①碳酸盐一般不溶于水。如碳酸钙不溶于水。
②碳酸钙能与二氧化碳、水反应生成碳酸氢钙[Ca(HCO3)2],碳酸氢钙易溶于水。
③碳酸氢钙受热易分解,生成碳酸钙、二氧化碳、水。
从物质组成角度分类,碳酸氢钙应属于(_____)。
A.氧化物 B.酸 C.碱 D.盐
写出碳酸氢钙受热分解的化学方程式__________________________。
(3)(提出问题)碳酸氢钙能与哪些物质反应呢?
(4)(假设与猜想)猜想I:能与盐酸反应
猜想lI:能与氢氧化钠反应
……………
(5)(设计实验并验证)
实验步骤 | 实验现象 | 结论 |
实验一:取丙中少量液体于试管中,滴加稀盐酸 | 有_________生成 | 猜想I成立 |
实验二:取丙中少量液体于试管中,滴加氢氧化钠溶液 | 有白色沉淀生成 | 猜想II成立 |
实验三:取丙中少量液体于试管中,加热 | 澄清液体又变浑浊 | 验证了资料描述 |
根据验证实验写出碳酸氢钙与盐酸反应的化学方程式______________。
(6)(讨论与反思)
该实验小组在实验中发现问题,并对问题进行不断探究。他们不但发现了新的物质,还了解了它的一些性质,并对生活中煮沸可以降低水的硬度、水垢的形成以及自然界中溶洞与钟乳石的形成有了更进一步的认识。