题目内容
【题目】根据已掌握实验室制取气体的有关知识,请结合图示回答下列问题。
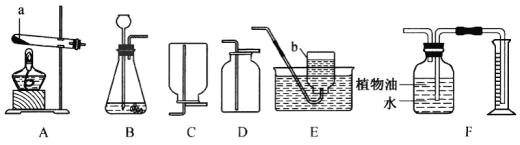
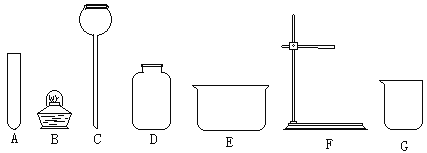
(1)请写出图中标号a、b仪器的名称:a_______;b_______。
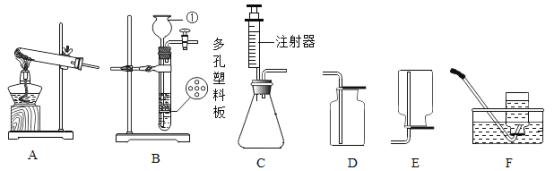
(2)实验室用双氧水溶液和二氧化锰混合制取氧气时,发生的反应的符号表达式为_______,反应的类型为_______反应。选用的发生装置是_______ (填装置序号)。
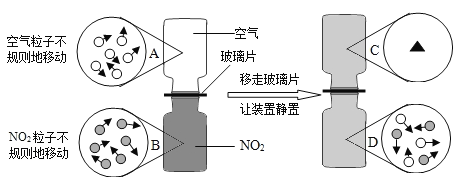
(3)F装置可用来测量生成的CO2气体的体积,在水面上放一层植物油的目的是__________,植物油上方原有的空气对实验的结果_________(填“有”或“没有”)明显影响。最终若俯视量筒中水,读数为20.0 mL,则氧气的体积将________(填“大于”“小于”或“等于”)20.0 mL。
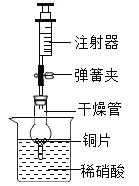
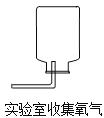
(4)1909年化学家哈伯在实验室首次将氮气和氢气在一定条件下合成了氨气(NH3)。常温下,氨气是一种无色有刺激性气味的气体,密度小于空气,极易溶解于水。实验室常用加热固体硫酸钱和固体熟石灰的混合物来制取氨气,发生装置应选用________装置,同学们一致认为,选择D装置收集氨气不合理,理由是__________。
【答案】试管 集气瓶 ![]() 分解 B 防止CO2气体溶于水 没有 小于 A 氨气的密度比空气小,故应选择C装置来收集
分解 B 防止CO2气体溶于水 没有 小于 A 氨气的密度比空气小,故应选择C装置来收集
【解析】
(1)根据对仪器的性状和作用可以判断a是试管,作反应容器,b是集气瓶,用来收集和贮存气体;
(2)用双氧水溶液和二氧化锰混合制取氧气,反应的化学式表达式是:![]() ,该反应由一种物质分解生成两种物质,属于分解反应,该反应不需加热,属于固液常温型,故选发生装置B;
,该反应由一种物质分解生成两种物质,属于分解反应,该反应不需加热,属于固液常温型,故选发生装置B;
(3)图F是采用排水法测二氧化碳的体积,用量筒测量水的体积从而测二氧化碳的体积;二氧化碳能溶于水,所以要在水的上方放一层植物油,防止二氧化碳溶于水.排水法测气体体积的原理是利用排出水的体积和进入装置中的气体的体积相等的原理进行的,所以在没有二氧化碳生成时,盛水的集气瓶中压强和外界大气压是相等,当有二氧化碳气体生成时,集气瓶内气体压强增大,将水排出,所以油上方的空气对实验结果没有影响;俯视液面读数偏大,实际水的体积小于20.0mL,所以氧气的体积小于20.0mL;
(4)用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,属于固体加热型,故选发生装置A,氨气不能用 向上排空气法收集,是因为氨气的密度比空气小;
故答案为:(1)试管;集气瓶;
(2)![]() ;分解反应;B;
;分解反应;B;
(3)防止CO2溶于水且与水反应;没有;小于;
(4)A;氨气的密度比空气小.

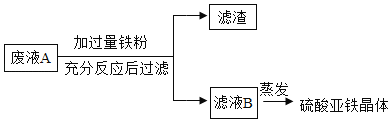
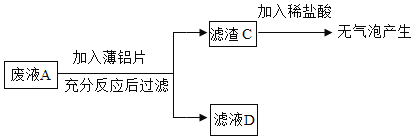
【题目】工业上常利用石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3的流程如下:

已知:①反应1为:6Cl2 + 6Ca(OH)2 =Ca(ClO3)2 + 5CaCl2 + 6H2O。②有关物质在常温下的溶解度如下:
物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
溶解度/g | 209.0 | 74.5 | 7.3 | 34.0 |
回答下列问题:
(1)在实验中两次涉及过滤操作,完成此操作需要的玻璃仪器有烧杯、玻璃棒、 ________,该操作中玻璃棒的作用是__________。
(2)Ca(ClO3)2的名称是___________。对于反应1,参加反应的Cl2中有一部分Cl的化合价升高,另一部分降低,则化合价升高的Cl与化合价降低的Cl 的个数比为_________。
(3)反应2为KCl与Ca(ClO3)2发生的复分解反应,该反应能发生的主要原因是_____。溶液A中含有的溶质为CaCl2和_________(填化学式)。
(4)上述流程中析出的KClO3晶体表面通常吸附有Ca2+、Cl-等杂质离子,过滤时洗涤KClO3晶体,应选用下列中的___________饱和溶液(填编号)。
A KCl B CaCl2 C KClO3 D Na2CO3