题目内容
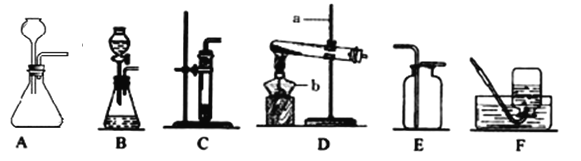
【题目】下面是实验室制取和收集气体的装置,请按要求作答:
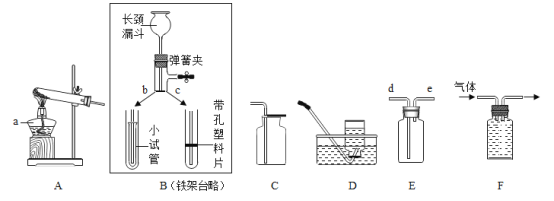
(1)仪器a的名称是______________ 。
(2)用B装置制取气体时当上部与下部c对接时,组合成装置的优点是______________ 。
(3)从装置A~D中选择:加热KMnO4制取并收集O2,应选用图中的________(填字母),其反应化学方程式是______________ 。若制取的O2用F装置排水法收集,请将图F补画完整_______。
(4)第二组同学接着又做了如图的实验——
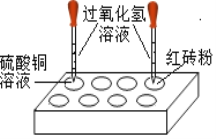
寻找过氧化氢分解的新催化剂。白色点滴板是带有空穴的白色瓷板,可用作微型化学反应。在将一定量的红砖粉、硫酸铜溶液……分别加入点滴板中,再分别滴入过氧化氢溶液(如图所示),观察到过氧化氢溶液产生气泡的速率加快。据此现象得出结论:红砖粉、硫酸铜溶液等也能作过氧化氢分解的催化剂。小红认为不正确,理由一:未探究它们的质量是否不变;理由二:__________。白色点滴板作为反应容器的优点_____________。写出硫酸铜和过氧化氢混合制取氧气的方程式_____________。
【答案】酒精灯 可随时使反应发生或停止 AD 2KMnO4 ![]() K2MnO4 + MnO2 + O2↑ 右端导气管是长导气管 未探究它们的化学性质是否不变 节约药品,便于观察现象 2H2O2
K2MnO4 + MnO2 + O2↑ 右端导气管是长导气管 未探究它们的化学性质是否不变 节约药品,便于观察现象 2H2O2![]() 2H2O + O2↑
2H2O + O2↑
【解析】
(1)仪器a是酒精灯。
(2)用B装置制取气体时当上部与下部c对接时,组合成装置的优点是可控制反应的发生或停止。
(3)加热固体制取气体选择发生装置A,氧气不易溶于水,可用排水法收集,虽然也可用向上排空气法收集,但用排水法收集的气体较纯净,故选AD。高锰酸钾在加热时发生分解反应生成锰酸钾、二氧化锰、氧气。用F装置排水法收集收集氧气,氧气从左端进入,水从右端排出,右端的导气管是长导气管,当剩余的水减少时,便于排出。
(4)催化剂在化学反应前后化学性质不变。白色点滴板作为反应容器的优点是节约药品、便于观察现象。过氧化氢在二氧化锰作催化剂的条件下发生分解反应生成水和氧气。

【题目】“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号 | 硫酸的质量分数 (均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式________________________________________。
(2)小兵用下图装置收集并测量氢气的体积,其中量筒的作用是_______________________,氢气应从________(填e或f或g)管通入。

【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】
(4)结论是___________________________________________。
【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分)
(5)下表是小兵第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应的快慢的变化并解释原因______________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。
_____________________________________。
【题目】化学小组围绕“铁丝在氧气中燃烧现象及产物”的问题,进行了相应的探究活动。
活动1:“火星四射”的现象与铁丝含碳量的关系
实验操作 | 实验现象 | 实验结论 |
实验1:取直径0.20mm,含碳0.1%的铁丝,在氧气中燃烧 | 零星火星 | 铁丝燃烧的符号表达式是___________________ “火星四射”与铁丝含碳量的关系是_____________。 |
实验2:取直径_____mm,含碳0.3%的铁丝,在氧气中燃烧 | 较明显的火星四射 |
活动2:黑色固体中是否含有铁?
资料:①铁粉和四氧化三铁为黑色固体,均具有磁性,可用磁铁吸引。
②铁、四氧化三铁均能溶于稀盐酸(即:铁 + 盐酸 →氯化亚铁 + 氢气;四氧化三铁+盐酸→氯化铁+氯化亚铁+水)
③氯化亚铁溶液为浅绿色,氯化铁溶液为黄色。
小明质疑小刚用磁铁来检验黑色固体是否含有铁的方案,其理由是________;同学们都认可了下列实验方案:
实验操作 | 实验现象 | 实验结论 |
取少量黑色固体于试管中,加入一定量__________,放置一段时间 | 有气泡产生,溶液由无色变为黄色 | 黑色固体中含有铁 |