题目内容
【题目】我国的航空航天领域已经处于世界领先的水平,请回答下列问题:
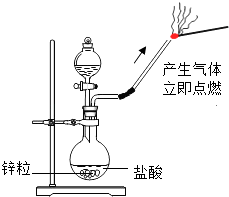
(1)2008年9月27日,太空第一次留下了“中国人的脚印”.我国研制的航天员舱外服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),它不可能具有的化学性质是(填字母序号).
A.与二氧化碳反应
B.使酚酞变红
C.与盐酸反应
D.与锌粒反应
(2)火箭是航天器的运载工具,火箭用液氢做燃料,请写出液氢燃烧的化学方程式 , 该反应是将能转化为热能.
(3)2011年我国首个火星探测器“萤火一号”将踏上访问火星的旅程.太阳能帆板是探测器的重要部件,其制作材料之一的高纯硅(Si)是用氢气与四氯化硅(SiCl4)在高温条件下反应生成硅和氯化氢,该反应的化学方程式为: , 属于反应.
【答案】
(1)D
(2)2H2+O2 ![]() 2H2O,化学
2H2O,化学
(3)SiCl4+2H2 ![]() Si+4HCl,置换
Si+4HCl,置换
【解析】(1)因为氢氧化钠性质和氢氧化锂相似,因此氢氧化锂不可能与锌粒反应.故填:D.
(2)液氢燃烧的化学方程式为:2H2+O2 ![]() 2H2O,该反应是将化学能转化为热能.故填:2H2+O2
2H2O,该反应是将化学能转化为热能.故填:2H2+O2 ![]() 2H2O;化学.
2H2O;化学.
(3)高温条件下,四氯化硅能和氢气反应生成硅和氯化氢,反应的化学方程式为:SiCl4+2H2 ![]() Si+4HCl,属于置换反应.故填:SiCl4+2H2
Si+4HCl,属于置换反应.故填:SiCl4+2H2 ![]() Si+4HCl;置换.
Si+4HCl;置换.
【考点精析】关于本题考查的书写化学方程式、文字表达式、电离方程式和氢气的化学性质与燃烧实验,需要了解注意:a、配平 b、条件 c、箭号;化学性质:可燃性(用途:高能燃料;氢氧焰焊接,切割金属);还原性(用途:冶炼金属)(小结:既有可燃性,又有还原性的物质 H2、C、CO)才能得出正确答案.

【题目】某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验: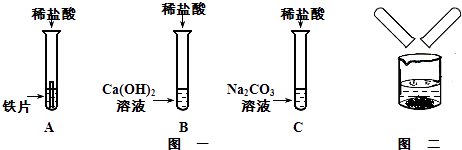
(1)A试管中滴加稀盐酸后,可观察到的现象是 , 发生反应的化学方程式为;
(2)写出B试管中反应的化学方程式;
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究:
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
丁同学猜想: .
(4)【查阅资料】NaCl、CaCl2溶液均呈中性.
【交流讨论】甲同学认为同学的猜想一定不正确,理由是: .
(5)【设计实验】乙、丁两位同学分别设计如下实验验证自己的猜想:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
乙 | 取少量滤液于试管中,向其中滴加无色酚酞试液 | 无明显现象 | 猜想正确 |
丁 | 取少量滤液于试管中,向其中滴加稀盐酸 | 猜想正确 |
(6)【反思评价】实验结束后,甲同学认为(填“乙”或“丁”)同学的实验结论错误,原因是 .