题目内容
【题目】向50.0g 8.0%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应,此时溶液pH=7。
(1)求反应前氢氧化钠溶液中溶质的质量;
(2)求反应后生成硫酸钠的质量。
【答案】(1)4.0g (2)7.g
【解析】(1)根据“溶液质量×溶质质量分数=溶液中溶质的质量”就可计算出反应前氢氧化钠溶液中溶质的质量;
(2)根据氢氧化钠与硫酸反应的化学方程式和参与反应的NaOH的质量,列出比例式,就可计算出反应后生成硫酸钠的质量.
(1)反应前氢氧化钠溶液中溶质的质量=50.0g×8.0%=4.0g;
(2)设反应后生成硫酸钠的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O
80 98 142
4.0g x
∴![]() ,
,
解之得:x=7.1g.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
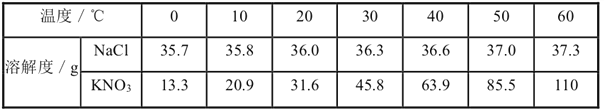
【题目】下表列出了固体物质A在不同温度时的溶解度:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
(1)70℃时,向盛有100g水的烧杯中加入30g固体A,充分溶解形成的是______________(填“饱和”或“不饱和”)溶液,再将烧杯内物质温度降至20℃,此时溶液中溶质与溶剂的质量比为_____________(填最简整数比);
(2)通过对上表数据的分析,物质A的溶解度曲线应是右图中的___________(填“甲”或“乙”);

(3)80℃时,配制一定量A物质的溶液,将其降温到60℃,是否有固体析出?____________(填“有”、 “没有”或“不确定”)。