题目内容
【题目】氯化钠是日常生活的必需品,也是重要的化工原料,海水“晒盐”得到的是粗盐。粗盐除含NaCl 外,还含有少量 MgCl2、CaCl2、Na2SO4以及泥沙等杂质
(1)有关粗盐提纯的实验操作合理的是___(填序号)。
A 溶解前用玻璃棒研磨大颗粒粗盐
B 过滤时液体的液面要低于滤纸边缘
C 蒸发时要不断搅拌直至水分全部蒸干
D 实验结束用玻璃棒把固体转移到纸上,称量后,回收到指定容器中
(2)粗盐进行精制,流程如图。
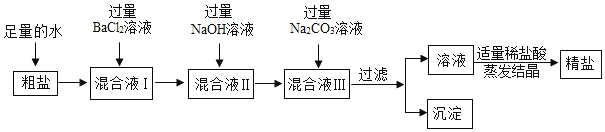
温合液Ⅲ经过“过滤”操作,得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、___(填化学式)
(3)加入过量的NaOH溶液的目的为___(用化学方程式表示)。
(4)实验所得精盐的质量大于粗盐中NaCl的质量,原因是___。
【答案】BD CaCO3和BaCO3 MgCl2+2 NaOH=2NaCl+ Mg(OH)2↓ 除杂质过程中新生成了氯化钠
【解析】
(1)
A、研磨大颗粒粗盐应该用研钵和杵,选项操作不合理;
B、过滤时要使液体的液面低于滤纸边缘,选项操作合理;
C、蒸发时要用玻璃棒不断搅拌,防止局部温度过高,造成液滴飞溅,加热到出现较多量固体时停止加热,利用蒸发皿的余热蒸干滤液,不能加热直至水分全部蒸干,选项操作不合理;
D、实验结束用玻璃棒把固体转移到纸上,称量后,回收到指定容器中,选项操作合理,故符合题意的填BD;
(2)氯化钡和硫酸钠反应生成硫酸钡沉淀,氢氧化钠和氯化镁反应生成氢氧化镁沉淀,碳酸钠和氯化钙反应生成碳酸钙沉淀,碳酸钠还和过量的氯化钡反应生成碳酸钡沉淀,所以混合液III经过“过滤”操作,得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、CaCO3和BaCO3,故填CaCO3和BaCO3;
(3)加入过量的NaOH溶液的目的是除尽溶液中的镁离子,使氯化镁和氢氧化钠完全反应生成氢氧化镁沉淀和氯化钠,方程式故填MgCl2+2 NaOH=2NaCl+ Mg(OH)2↓;
(4)在除去MgCl2、CaCl2、Na2SO4杂质的过程中,以及最后酸化过程中都新生成了氯化钠,使得实验所得精盐的质量大于粗盐中NaCl的质量,故填除杂质过程中新生成了氯化钠。

【题目】为测定某地石灰石中碳酸钙的质量分数,某兴趣小组将一定质量的石灰石样品粉碎后分成两等份,进行如下实验:
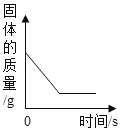
(1)一份放于烧杯中,向烧杯中逐渐加入某一浓度的盐酸,反应过程测得剩余固体质量与加入盐酸的质量关系如图所示(石灰石中的杂质不与盐酸反应,也不溶与水)。请回答下列问题:
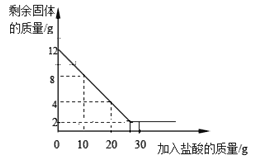
①石灰石样品中碳酸钙的质量分数________;
②通过计算求所用盐酸的溶质质量分数为__________。
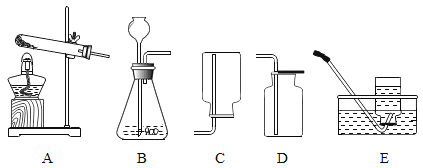
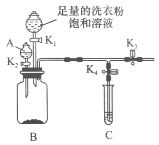
(2)另一份进行如下图所示的实验:把产生的CO2气体用足量的烧碱溶液吸收,同时测量B瓶烧碱溶液增加的质量,结果如下表所示:
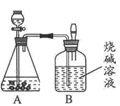
时间/分 | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
B增加的质量 | 0 | 2 | 3 | 4 | 4.6 | X | 4.6 |
①右上表中,第5分钟时,x=______________;
②该实验测得样品中碳酸钙的质量分数_________(填大于、小于或等于)另一实验,其原因可能是______________________________。
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
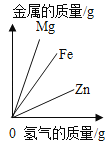
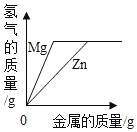
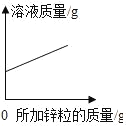
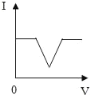
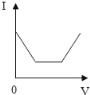
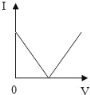
Mg、Zn、Fe与稀盐酸反应 | 等质量等质量分数的盐酸与足量的镁粉、锌粉 | 将铜片加入一定量的硝酸银溶液中 | 向一定质量的氯化锌和盐酸溶液中加入锌粒 |
A. A B. B C. C D. D