题目内容
【题目】某兴趣小组欲探究Al、Cu、Ag三种金属的活动性顺序,进行了如下实验:
(1)请填写实验报告:
(实验目的)探究Al、Cu、Ag三种金属的活动性顺序
(实验过程)
实验验内容 | 实验现象 | 解释或化学方程式 |
①将一根用砂纸打磨干净的铝丝放入硫酸铜溶液中 | 观察到铝丝表面有红色物质生成,溶液颜色变浅 | 用砂纸打磨铝丝的目的是________ |
②再将一根用砂纸打磨干净的铜丝放入________溶液中 | 观察到铜丝表面有银白色物质生成,溶液颜色由无色变为蓝色 | 化学方程式为_________ |
(实验结论)Al、Cu、Ag三种金属的活动性顺序由强到弱为_________;
(2)在确定了活动性后,同学们继续实验,向一定质量的硝酸银和硝酸铜的混合溶液中加入一定质量的铝粉,充分反应后过滤,得液体A和固体B。向固体B中加入稀盐酸,有气泡产生。根据此实验现象分析:所得液体A中除水外一定含有的物质是_______,固体B中一定含有的物质是_________。
【答案】除去铝表面的氧化膜 硝酸银 ![]() Al>Cu>Ag 硝酸铝 Al、Cu、Ag
Al>Cu>Ag 硝酸铝 Al、Cu、Ag
【解析】
(1)实验过程:
①解释或化学方程式:铝的化学性质比较活泼,在常温下容易与空气中的氧气反应生成一层致密的氧化铝薄膜,用砂纸打磨铝丝的目的是:除去铝表面的氧化膜;
②实验现象为:观察到铜丝表面有银白色物质生成,溶液颜色由无色变为蓝色,说明铜与硝酸银反应生成了硝酸铜和银,故实验内容为将一根用砂纸打磨干净的铜丝放入硝酸银溶液中,该反应的化学方程式为:![]() ;
;
实验结论:
铝能与硫酸铜反应生成硫酸铝与铜,说明在金属活动性顺序里,铝位于铜之前,铜能与硝酸银反应生成硝酸铜和银,说明在金属活动性顺序里,铜位于银之前,故Al、Cu、Ag三种金属的活动性顺序由强到弱为Al>Cu>Ag;
(2)向一定质量的硝酸银和硝酸铜的混合溶液中加入一定质量的铝粉,铝先和硝酸银反应生成硝酸铝和银,待硝酸银完全反应后,再和硝酸铜反应生成硝酸铝和铜,充分反应后过滤,得液体A和固体B。向固体B中加入稀盐酸,有气泡产生,说明固体B中含铝,说明铝过量,硝酸银和硝酸铜已经完全反应,故所得液体A中除水外一定含有的物质是硝酸铝,固体B中一定含有的物质是Al、Cu、Ag。

【题目】如下表所示,已知A与一定量的B反应生成C和D。
物质 | A | B | C | D |
|
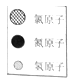
微观示意图 |
|
|
|
|
(1)参加反应的A和B个数比为_____。
(2)该反应中化合价升高的元素是_____。
(3)若在该反应中继续通入B,则D会与B继续反应产生一种氮肥,请写出此时A与B反应的总化学方程式:_____。