��Ŀ����
����Ŀ����һ��������п�ۼ���Mg��NO3��2��AgNO3��Cu��NO3��2�Ļ����Һ�У���ַ�Ӧ����ˣ��õ��������Һ��������Һ�����ͼ���п�۵�������ϵ��ͼ��ʾ���������ʾ����п�۵���������
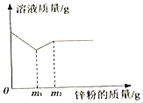
��1��������п�۵�����С��m1ʱ����Һ������Ϊʲô���٣�_____
��2��������п�۵�������m1��m2gʱ����Ӧ�Ļ�ѧ����ʽΪ_____��
��3����������п�۵���������m2ʱ�������ù����еμ�ϡ����_____����С����ޡ�������ð����
���𰸡�п���������ķ�Ӧ��������п���������ŷ�Ӧ������Һ������С Zn+Cu��NO3��2��Cu+Zn��NO3��2 ��
��������
��1���������˳���У�������ǰ��Ľ������ܺ�ϡ�����ϡ���ᷴӦ�����κ�����������ǰ��Ľ������ܰ����ں���Ľ�������������Һ���û��������ҽ�����Բ��Խ��ӦԽ��������һ��������п�ۼ���Mg(NO3)2��AgNO3��Cu(NO3)2�Ļ����Һ�У����ȷ�����Ӧ��Zn+2AgNO3=2Ag+Zn(NO3)2����AgNO3��ȫ��Ӧ��п����Cu(NO3)2��Һ��Ӧ��Zn+Cu(NO3)2=Zn(NO3)2 + Cu��������п�۵�����С�� m1 ʱ����п����������Ӧ��������п���������ŷ�Ӧ������Һ������С��
�ʴ�Ϊ��п���������ķ�Ӧ��������п���������ŷ�Ӧ������Һ������С��
��2��������п�۵�������m1��m2gʱ����п������ͭ��Ӧ��������п��ͭ����Ӧ�Ļ�ѧ����ʽΪ��Zn+Cu(NO3)2=Zn(NO3)2 + Cu��
���Zn+Cu��NO3��2��Cu+Zn��NO3��2��
��3��������п�۵���������m2ʱ��п���������ù����к������ɵ�����ͭ��������п�������ù����еμ�ϡ���ᣬп�����ᷴӦ�����Ȼ�п�������������ݲ�����
�����

 ��У����ϵ�д�
��У����ϵ�д�