题目内容
【题目】实验是学习化学的一种重要途径
(一)、实验室用下图所示装置制取并收集气体
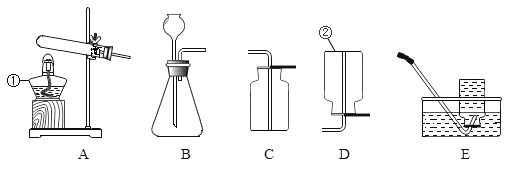
请回答下列各题:
(l)仪器① 的名称_________,②的名称__________。
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是_______________(填序号),反应的化学方程式是____;若用排水法收集氧气时不能刚有气泡就开始收集,原因是_______________。
(3)既能收集氧气也能收集二氧化碳气体的装置是______(填序号),检验二氧化碳气体是否收集满的方法是__________________;检验瓶中气体是否为二氧化碳可用_____________(填药品名称)。
(4)乙炔(C2H2)气体可用电石(CaC2块状固体)和水反应来制取,化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑,实验室制取乙炔(C2H2)气体的发生装置应选用_____(填序号)。
(二)、某化学兴趣小组的同学利用下图微型实验装置进行探究实验。
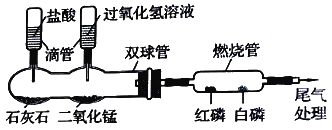
(1)请写出一个双球管中可能反应的化学方程式__________________________。
(2)挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,据此现象可说明燃烧需要的条件是_________。
(3)相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气最多的是_________。
【答案】 酒精灯 集气瓶 A 2KMnO4 ![]() K2MnO4+MnO2+O2↑ 刚开始冒出的气体中含有空气,会使收集的气体不纯 C 将一根燃着的木条靠近集气瓶口,若熄灭,则已收集满 澄清石灰水 B 2H2O2
K2MnO4+MnO2+O2↑ 刚开始冒出的气体中含有空气,会使收集的气体不纯 C 将一根燃着的木条靠近集气瓶口,若熄灭,则已收集满 澄清石灰水 B 2H2O2 ![]() 2H2O+O2↑(或CaCO3+2HCl=CaCl2+H2O+CO2↑) 与氧气接触,温度要达到可燃物的着火点 磷(或P)
2H2O+O2↑(或CaCO3+2HCl=CaCl2+H2O+CO2↑) 与氧气接触,温度要达到可燃物的着火点 磷(或P)
【解析】本题主要考查常见气体的发生装置与收集装置的探究,燃烧条件的探究,根据化学方程式的计算。发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择。
一、(l)仪器① 的名称酒精灯,②的名称集气瓶。
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以应选用发生装置是A,高锰酸钾加热生成了锰酸钾和二氧化锰和氧气,反应的化学方程式是2KMnO4 ![]() K2MnO4+MnO2+O2↑;若用排水法收集氧气时不能刚有气泡就开始收集,原因是刚开始冒出的气体中含有空气,会使收集的气体不纯;
K2MnO4+MnO2+O2↑;若用排水法收集氧气时不能刚有气泡就开始收集,原因是刚开始冒出的气体中含有空气,会使收集的气体不纯;
(3)氧气、二氧化碳的密度比空气大,氧气不易溶于水,二氧化碳能溶于水,所以既能收集氧气也能收集二氧化碳气体的装置是C,检验二氧化碳气体是否收集满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明集满;二氧化碳能使澄清石灰水变浊,检验瓶中气体是否为二氧化碳可用澄清石灰水;
(4)实验室制取甲烷的反应物是固体和液体,反应条件是常温,所以实验室制取乙炔(C2H2)气体的发生装置应选用B。
二、(1)双球管中涉及两个反应,分别为过氧化氢在二氧化锰的催化下生成水和氧气,另一反应为碳酸钙和盐酸反应生成二氧化碳、氯化钙以及水,对应的化学方程式分别为2H2O2 ![]() 2H2O+O2↑、CaCO3+2HCl=CaCl2+H2O+CO2↑;
2H2O+O2↑、CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,都有可燃物,都接触氧气,但是由于着火点不同,所以现象不同,由此可说明燃烧需要与氧气接触,温度要达到可燃物的着火点的条件;
(3)相同质量的磷、铁、镁分别在氧气中完全燃烧,设:消耗的可燃物的质量均为mg,对应的消耗的氧气的质量分别为x、y、z。
4P+5O2![]() 2P2O5
2P2O5
124 160
mg x
![]() =
=![]() x≈1.29mg
x≈1.29mg
3Fe+2O2![]() Fe3O4
Fe3O4
168 64
mg y
![]() =
=![]() y≈0.38mg
y≈0.38mg
2Mg+O2![]() 2MgO
2MgO
48 32
mg z
![]() =
=![]() z≈0.67mg
z≈0.67mg
所以消耗氧气最多的是磷(P)。

【题目】小红同学取某地石灰石样品12.5g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
请计算:
(1)m的值;
(2)石灰石样品中碳酸钙的质量分数;
(3)所用稀盐酸溶质的质量分数是多少?(要求写出计算过程)