题目内容
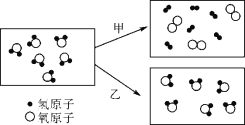
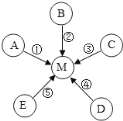
【题目】A,B均为纯净物,C,D,E均为混合物;①~⑤五条途径(见如图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,工业上可通过途径④来生产M,自然界可通过途径⑤来提供M;途径①、②、③反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂.
(1)M的化学式为________________,N的化学式为__________________;
(2)常温下,B为固态,C为液体,写出途径③反应的化学式表达式_____________________,属于_____________反应(填反应类型)
(3)工业上需要大量的M时,一般采用的方法是________________;主要是利用____________不同而实现分离的目的。
(4)途径⑤提供M在自然界中被称为__________________.
【答案】![]()
![]()
![]() 分解反应 分离液态空气 沸点 光合作用
分解反应 分离液态空气 沸点 光合作用
【解析】
根据A、B均为纯净物,C、D、E均为混合物,①~⑤五条途径都会产生M,实验室可利用途径①、②、③反应来制取M,所以M是氧气,常温下,A、B为固体,C为液体,所以C是过氧化氢溶液,在途径①反应生成的一种物质N可作为途径②、③反应的催化剂,所以B是氯酸钾,A是高锰酸钾,高锰酸钾生成的二氧化锰加快了氯酸钾的分解速率,工业上可通过途径④来生产![]() ,自然界可通过途径⑤来提供
,自然界可通过途径⑤来提供![]() ,所以途径④是分离液态空气,途径⑤是光合作用,然后将推出的物质进行验证即可。
,所以途径④是分离液态空气,途径⑤是光合作用,然后将推出的物质进行验证即可。
(1)A、B均为纯净物,C、D、E均为混合物,①~⑤五条途径都会产生M,实验室可利用途径①、②、③反应来制取M,所以M是氧气,常温下,A、B为固体,C为液体,所以C是过氧化氢溶液,在途径①反应生成的一种物质N可作为途径②、③反应的催化剂,所以B是氯酸钾,A是高锰酸钾,高锰酸钾生成的二氧化锰加快了氯酸钾的分解速率,工业上可通过途径④来生产![]() ,自然界可通过途径⑤来提供O2,所以途径④是分离液态空气,途径⑤是光合作用,经过验证,推导正确,所以M的化学式为:
,自然界可通过途径⑤来提供O2,所以途径④是分离液态空气,途径⑤是光合作用,经过验证,推导正确,所以M的化学式为:![]() ,N的化学式为:
,N的化学式为:![]() ;
;
(2)途径③为过氧化氢在二氧化锰的催化作用下加热生成水和氧气,化学式表达式为:![]() ,该反应由一种反应物反应生成两种生成物,属于分解反应;
,该反应由一种反应物反应生成两种生成物,属于分解反应;
(3)工业上需用大量氧气时,主要利用氧气和氮气的沸点不同,采用加压、降温的方法使空气液化,然后再蒸发掉氮气,即分离液态空气,就能得到大量氧气;
(4)途径⑤提供 M 在自然界中被称为光合作用。

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】已知: ![]() 。如图表示向一定质量的CuO中通入CO后,加热的过程中某变量y随时间的变化结果。y表示的是
。如图表示向一定质量的CuO中通入CO后,加热的过程中某变量y随时间的变化结果。y表示的是
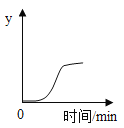
A.固体中铜元素的质量分数
B.参与反应的CO的质量
C.固体中氧元素的质量
D.气体中碳元素的质量
【题目】小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”这一命题,他设计并完成了下表所示的探究实验:
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验一 | 将氯酸钾加热至熔化,伸入带火星的木条 | 木条复燃 | 氯酸钾受热分解能产生氧气,但是_____ | 二氧化锰是氯酸钾受热分解的催化剂 |
实验二 | 加热二氧化锰,伸入带火星的木条, | 木条不复燃 | 二氧化锰受热不产生氧气。 | |
实验三 | _____,伸入带火星的木条 | 木条迅速复燃 | 二氧化锰能加快氯酸钾的分解速度。 | |
(1)请你帮小明同学填写上表中未填完的空格。
(2)写出氯酸钾受热分解的文字表达式:_____,在小明的探究实验中,“实验一”和“实验二”起的作用是_____;
(3)小英同学认为仅由上述实验还不能完全得出表内“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
①实验操作中包含了两次称量,其目的是_____;
②实验是要证明在反应前后,二氧化锰的_____不变。