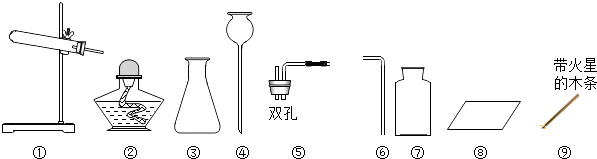
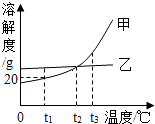
��Ŀ����
����Ŀ��������һ�ֱ������Ȼ��Դ��Ҫ������������ֹ��Ⱦ������ 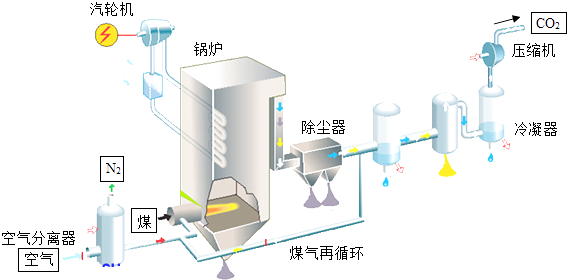
��1������Һ�������ɻ�õ������������壬����������������˵������ ��
��2������Ĥ���뼼������һ��ѹ�����ÿ���ͨ�����и����������ܵı�Ĥ���ܵõ��������ϸߵĸ����������ù��̷����仯��
��3��ijȼú�糧����ȼ�ռ���ԭ��ͼ��ͼ��ʾ�� �ٸ���ȼ������ͨȼ����ȣ����ṩ�����O2 �� ʹ��¯�е�CO���ȼ�գ���д��COȼ�յĻ�ѧ����ʽ����
�ڲ��øü��������ڶ�CO2�����������ã�����̼�ŷţ���õ�CO2�������Ƹɱ����ɱ�����;֮һ�� �� ��CO2Ҳ����NaOH��Һ����д����Ӧ�Ļ�ѧ����ʽ����
�۲���ͼ�й��գ�����ʹúȼ�ղ����ĵ��������������ŷ���������½����Ӷ���Ч��ֹ������γɣ�
���𰸡�
��1����������ѧ���ʲ�����
��2������
��3��2CO+O2 ![]() 2CO2���������2NaOH+CO2�TNa2CO3+H2O����������
2CO2���������2NaOH+CO2�TNa2CO3+H2O����������
���������⣺��1��������Ҫ���ɵ�����������ɵģ����Է���Һ�������ɻ�õ����������������壬����������������˵�������Ļ�ѧ���ʲ����ã����Դ��ǣ���������ѧ���ʲ����ã���2������Ĥ���뼼������һ��ѹ�����ÿ���ͨ�����и����������ܵı�Ĥ���ܵõ��������ϸߵĸ����������ù���û�в����µ����ʣ����Է������������仯�����Դ��ǣ���������3����CO�������ڵ�ȼ�����������ɶ�����̼����ȼ�յĻ�ѧ����ʽΪ��2CO+O2 ![]() 2CO2�����Դ��ǣ�2CO+O2
2CO2�����Դ��ǣ�2CO+O2 ![]() 2CO2���ڸɱ��ǹ���Ķ�����̼���ɱ�����ʱҪ������Χ�������ȣ����Ըɱ�������������������������ƺͶ�����̼��Ӧ����̼���ƺ�ˮ���䷴Ӧ�Ļ�ѧ����ʽΪ��2NaOH+CO2�TNa2CO3+H2O�����Բ�CO2Ҳ����NaOH��Һ�����Դ��ǣ��������2NaOH+CO2�TNa2CO3+H2O�����γ������������Ҫ�Ƕ�������͵������úȼ�ղ����ĵ�������Ͷ���������Ժ�����������Һ��Ӧ���ڶ�CO2�����������õ�ͬʱҲ�����յ�������Ͷ����������Դ��ǣ���������
2CO2���ڸɱ��ǹ���Ķ�����̼���ɱ�����ʱҪ������Χ�������ȣ����Ըɱ�������������������������ƺͶ�����̼��Ӧ����̼���ƺ�ˮ���䷴Ӧ�Ļ�ѧ����ʽΪ��2NaOH+CO2�TNa2CO3+H2O�����Բ�CO2Ҳ����NaOH��Һ�����Դ��ǣ��������2NaOH+CO2�TNa2CO3+H2O�����γ������������Ҫ�Ƕ�������͵������úȼ�ղ����ĵ�������Ͷ���������Ժ�����������Һ��Ӧ���ڶ�CO2�����������õ�ͬʱҲ�����յ�������Ͷ����������Դ��ǣ���������
�����㾫����������Ĺؼ�������������ijɷּ����ɷֵ�������������֪ʶ�����տ����ǻ���O2Լռ1/5����֧��ȼ�գ�N2Լռ4/5����֧��ȼ�գ�Ҳ����ȼ�գ�������ˮ���Լ��Է��ο�����Ⱦ�Ĵ�ʩ�����⣬�˽������Ⱦ��������ǿ����������⣬���ƻ���״����ʹ�������Դ�������ķ�����������������ŷţ�����ֲ�������֡��ֲݵȣ�

 ��У����ϵ�д�
��У����ϵ�д�