题目内容
(2010?工业园区模拟)(本题有a、b两小题,考生任选一题解答.若两题都解,则以a小题计分)a.工业上常用煅烧石灰石的方法制取生石灰,所得的生石灰一般为白色块状物,其应用非常广泛.试写出:
(1)工业上煅烧石灰石制取生石灰的化学方程式:;
(2)生石灰常用作食品干燥剂,其干燥时发生的化学反应方程式:;
(3)将生石灰用水调成20%的石灰乳,涂刷墙面和地面能对畜禽栏舍进行消毒.用于消毒的该浆状物要现配现用,放置过久,就要失效,其原因是(用化学方程式表示).
b.铁是我们日常生活中应用最为广泛的金属,试完成下列填空:
(1)生活中的铁制用品常常会生锈,有人建议用稀硫酸除去铁制品表面的铁锈,有人则提出反对,反对用稀硫酸除去铁制品表面铁锈的理由是 (用化学方程式表忝).
(2)下列生活中的一些做法能防止铁生锈的举措是
A.将切过菜的刀用清水洗净后擦干 B.将不经常用的菜刀放在黑暗处
C.在铁制的门框、窗户上涂刷油漆 D.将自行车放在室外以方便取用.
【答案】分析:a、(1)煅烧石灰石会发生分解反应,生成物是氧化钙与二氧化碳;
(2)氧化钙和水反应生成氢氧化钙;
(3)氢氧化钙和二氧化碳反应生成碳酸钙和水;
b、(1)铁可与稀硫酸反应生成硫酸亚铁和氢气;
(2)根据铁生锈的条件进行分析,铁在有水和氧气并存时易生锈,防锈就是使铁不与水或氧气接触.
解答:解:a、(1)煅烧石灰石会发生分解反应,生成氧化钙与二氧化碳,这是工业制取二氧化碳的一种方式,化学方程式为CaCO3 CaO+CO2↑;
CaO+CO2↑;
(2)氧化钙能吸收水,和水反应生成氢氧化钙,常用作食品干燥剂,化学方程式为CaO+H2O=Ca(OH)2;
(3)生石灰可与水反应生成氢氧化钙,氢氧化钙可以杀菌消毒,氢氧化钙容易和空气中的二氧化碳反应生成碳酸钙,生成的碳酸钙不具有消毒性,化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;
b、(1)生活中的铁制用品常常会生锈,有人建议用稀硫酸除去铁制品表面的铁锈,有人则提出反对,因为铁可与稀硫酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4=FeSO4+H2↑;
(2)A、用后及时清洗擦干是常用的一种防止菜刀生锈的方法,故A正确.
B、把菜刀存放在黑暗的地方,为菜刀生锈提供了条件,会加速菜刀生锈,故B不正确.
C、涂油能使铁与水隔绝,起到防锈的作用,故C正确;
D、自行车长期放在室外,会加快自行车的生锈,故D错误.
故答案为:
a、(1)CaCO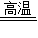 CaO+CO2↑;(2)CaO+H2O=Ca(OH)2;(3)Ca(OH)2+CO2=CaCO3↓+H2O;
CaO+CO2↑;(2)CaO+H2O=Ca(OH)2;(3)Ca(OH)2+CO2=CaCO3↓+H2O;
b、(1)Fe+H2SO4=FeSO4+H2↑;(2)AC.
点评:本题考查了除锈防锈的方法、碳酸钙氧化钙氢氧化钙之间的转化以及化学方程式的书写、,在解此类方程式的书写题时,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式.
(2)氧化钙和水反应生成氢氧化钙;
(3)氢氧化钙和二氧化碳反应生成碳酸钙和水;
b、(1)铁可与稀硫酸反应生成硫酸亚铁和氢气;
(2)根据铁生锈的条件进行分析,铁在有水和氧气并存时易生锈,防锈就是使铁不与水或氧气接触.
解答:解:a、(1)煅烧石灰石会发生分解反应,生成氧化钙与二氧化碳,这是工业制取二氧化碳的一种方式,化学方程式为CaCO3
 CaO+CO2↑;
CaO+CO2↑;(2)氧化钙能吸收水,和水反应生成氢氧化钙,常用作食品干燥剂,化学方程式为CaO+H2O=Ca(OH)2;
(3)生石灰可与水反应生成氢氧化钙,氢氧化钙可以杀菌消毒,氢氧化钙容易和空气中的二氧化碳反应生成碳酸钙,生成的碳酸钙不具有消毒性,化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;
b、(1)生活中的铁制用品常常会生锈,有人建议用稀硫酸除去铁制品表面的铁锈,有人则提出反对,因为铁可与稀硫酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4=FeSO4+H2↑;
(2)A、用后及时清洗擦干是常用的一种防止菜刀生锈的方法,故A正确.
B、把菜刀存放在黑暗的地方,为菜刀生锈提供了条件,会加速菜刀生锈,故B不正确.
C、涂油能使铁与水隔绝,起到防锈的作用,故C正确;
D、自行车长期放在室外,会加快自行车的生锈,故D错误.
故答案为:
a、(1)CaCO
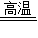 CaO+CO2↑;(2)CaO+H2O=Ca(OH)2;(3)Ca(OH)2+CO2=CaCO3↓+H2O;
CaO+CO2↑;(2)CaO+H2O=Ca(OH)2;(3)Ca(OH)2+CO2=CaCO3↓+H2O;b、(1)Fe+H2SO4=FeSO4+H2↑;(2)AC.
点评:本题考查了除锈防锈的方法、碳酸钙氧化钙氢氧化钙之间的转化以及化学方程式的书写、,在解此类方程式的书写题时,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
(2010?工业园区模拟)某兴趣小组围绕着“氢气在空气中的爆炸极限”进行探究,记录的现象和数据如下表所示:
(1)下列说法正确的是:______
A.点燃氢气和空气的混合气体不一定会发生爆炸
B.点燃氢气前不一定要检验氢气的纯度
C.点燃空气中氢气的体积分数在30%的混合气体会发生爆炸
D.只有绝对纯净的氢气,点燃后才不会发生爆炸
(2)已知:将氢气和氧气的体积按它们生成水时的化学计量数之比进行混合时,爆炸最剧烈.
现若设空气中氧气的体积分数为20%,其余都为氮气,试求:200L空气中混入多少升氢气时爆炸最剧烈?
| H2体积分数(%) | 5 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 空气体积分数(%) | 95 | 90 | 80 | 70 | 60 | 50 | 40 | 30 | 20 | 10 |
| 点燃时现象 | 不燃 不爆 | 弱爆炸 | 强爆炸 | 强爆炸 | 强爆炸 | 强爆炸 | 强爆炸 | 弱爆炸 | 安静 燃烧 | 安静 燃烧 |
A.点燃氢气和空气的混合气体不一定会发生爆炸
B.点燃氢气前不一定要检验氢气的纯度
C.点燃空气中氢气的体积分数在30%的混合气体会发生爆炸
D.只有绝对纯净的氢气,点燃后才不会发生爆炸
(2)已知:将氢气和氧气的体积按它们生成水时的化学计量数之比进行混合时,爆炸最剧烈.
现若设空气中氧气的体积分数为20%,其余都为氮气,试求:200L空气中混入多少升氢气时爆炸最剧烈?
(2010?工业园区模拟)已知五氧化二磷能和水反应生成相应的酸,该酸和硫酸、盐酸一样,能使酸碱指示剂变色,能与氢氧化钠发生中和反应.现若按图给出的条件进行实验,随着反应的进行,依次观察到下表中记录的实验现象,试选择表格下方的A、B、C等解释产生这些现象的原因(有多个要点时需一并选出).
A.过量的红磷燃烧后将集气瓶内空气中的氧气完全消耗
B.五氧化二磷与水反应生成磷酸
C.冷却后集气瓶内气体的压强减小
D.集气瓶内气体受热膨胀的体积大于刚开始燃烧时消耗的氧气的体积
E.红磷燃烧放出大量的热
F.红磷燃烧生成白色固体五氧化二磷
H.空气中氧气的含量约占空气体积的五分之一
I.磷酸能像盐酸一样使紫色石蕊试液变红色.

| 现象 | 原因 | ||
| 实验 刚开 始时 | 1 | 集气瓶中有大量白烟 | |
| 2 | 集气瓶发烫 | ||
| 3 | 插入烧杯中的导管口有气泡冒出 | ||
| 一段 时间 以后 | 4 | 烧杯中水溶液倒流回集气瓶中 | |
| 5 | 倒流回集气瓶中的溶液圼红色 | ||
| 6 | 最后进入集气瓶中液体的体积约占集气瓶容积的五分之一 | ||
B.五氧化二磷与水反应生成磷酸
C.冷却后集气瓶内气体的压强减小
D.集气瓶内气体受热膨胀的体积大于刚开始燃烧时消耗的氧气的体积
E.红磷燃烧放出大量的热
F.红磷燃烧生成白色固体五氧化二磷
H.空气中氧气的含量约占空气体积的五分之一
I.磷酸能像盐酸一样使紫色石蕊试液变红色.
