题目内容
某化学研究性学习小组的同学将43.75g石灰石(杂质SiO2不参加反应,也不溶于水)放入一定质量的某稀盐酸中,恰好完全反应,过滤(滤液损失不计),得到114g滤液,再向其中加入163.5g水,结果就得到了10%的溶液作为路面保湿剂.计算原稀盐酸中溶质的质量分数.
18.25%
试题分析:反应后溶液中溶质氯化钙的质量为(114g+163.5g)×10%=27.75g,设石灰石中碳酸钙的质量是x 反应的氯化氢质量是y 生成二氧化碳的质量是z
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 111 44
x y 27.75g z
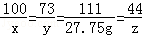
x=25g y=18.25g z=11g
则加入盐酸的质量为114g+11g﹣25g=100g,故所采用的盐酸溶质质量分数为:
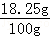 ×100%=18.25%
×100%=18.25%答:盐酸中溶质的质量分数为18.25%.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目

