题目内容
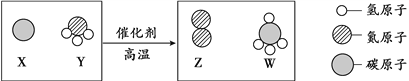
【题目】医疗上常用硫酸钡作透视肠的内服剂.俗称“钡餐”。一旦误将碳酸钡代替硫酸钡作“钡餐”,就会致人中毒,此时可服用硫酸镁溶液解毒。某化学兴趣小组用如下实验模拟了碳酸钡在胃液中的变化,并验证了硫酸镁解番的原理:
I.取一定量碳酸钡固体于烧杯中,逐滴加入188g稀盐酸至过量,并不断搅拌至固体完全溶解。
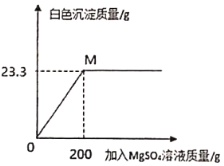
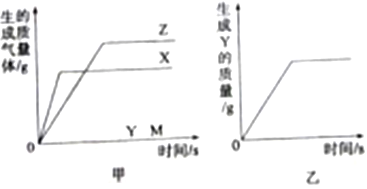
II.再向该烧杯中逐滴加入硫酸镁溶液,并不析搅拌,烧杯内产生白色沉淀质量与加入硫酸镁溶液的质量关系如图所示。
请你结合图像和提供的数据进行分析与计算。
(1)请你设计实验方案证明步骤I反应后的溶液中盐酸过量(只写出试剂名称)_____;
(2)通过计算确定硫酸镁溶液的溶质质量分数_____。(写出计算过程)
(3)请你计算M点所得溶液中氯化镁的溶质质量分数为_____。
【答案】紫色石蕊试剂 6% 2.5%
【解析】
碳酸钡可以与稀盐酸反应生成氯化钡、二氧化碳和水,加入过量的盐酸目的是使碳酸钡完全溶解,然后用硫酸镁与氯化钡反应生成沉淀,如图所示;刚开始时氯化钡过量,不断加入硫酸镁,沉淀一直产生,知道氯化钡完全反应完后,不再产生沉淀,完全反应的点是M点。
(1)设计实验方案证明步骤I碳酸钡和稀盐酸反应后的溶液中盐酸过量可以采用紫色石蕊试剂;若过量则显示为红色;故填:紫色石蕊试剂
(2)解:设硫酸镁的质量为X,氯化镁的质量为Y。
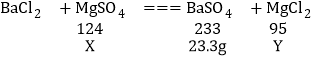
![]()
![]() ;
;![]()
硫酸镁溶液的溶质质量分数为:![]()
答:硫酸镁溶液的溶质质量分数为6%; 故填:6%
(3) M点时,硫酸镁和氯化钡完全反应,所得溶液中氯化镁的质量由(2)已经求出等于9.5g;根据硫酸钡的质量推求出碳酸钡的质量及产生二氧化碳气体的质量为: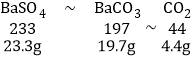
此时溶液的质量把所有加入的试剂全部加起来,以沉淀和其体形式脱离溶液体系的都减去。得其质量为:19.7g+188g+200g-23.3g-4.4g=380g
故M点所得溶液中氯化镁的溶质质量分数为:![]()
答:M点所得溶液中氯化镁的溶质质量分数为2.5% ;故填:2.5%

【题目】下列“课外实验”得出的结论错误的是
选项 | A | B | C | D |
课外 实验 |
|
|
|
|
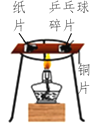
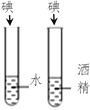
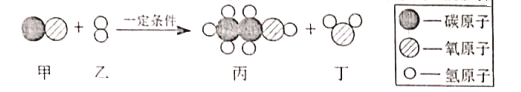
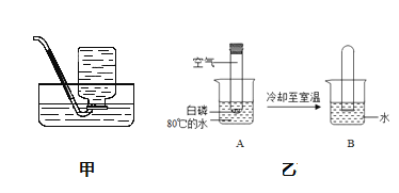
实验 结论 | 说明蜡烛 含有炭黑 | 说明有些花的色素 可做酸碱指示剂 | 不同物质着火点不同 | 说明同种溶质在不同种 溶剂里溶解性不同 |
A. AB. BC. CD. D