题目内容
【题目】生石膏[化学式为CaSO4·2H2O]是一种用途广泛的工业材料和建筑材料。工业上用含SO2的烟气制备生石膏的简要流程图如下:
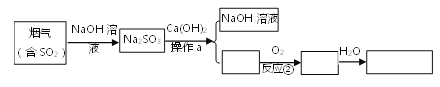
(1)在反应①时,常将NaOH溶液喷成雾状的原因是________。
(2)已知CaSO3不易溶于水,它属于________(填“酸”、“碱”、“盐”或“氧化物”),其中硫元素的化合价为______,反应②的化学方程式是_______。
(3)如果在实验室中进行分离操作a,所需的玻璃仪器有烧杯、玻璃棒和________。
(4)生产流程中生成的______可循环利用,节约成本。
【答案】 增大吸收面积,以加快反应速度 盐 +4 2CaSO3+O2=2CaSO4 漏斗 NaOH溶液
【解析】(1)在反应①时,常将NaOH溶液喷成雾状的原因是增大吸收面积,使反应物接触更充分,以加快反应速度,反应更彻底;(2) 由两种元素组成,且其中一种是氧的化合物叫氧化物。溶于水产生的阳离子只有氢离子的化合物是酸 。由金属或铵根和酸根组成的化合物叫盐,由金属或铵根和氢氧根组成的化合物叫碱。CaSO3属于盐,化合物中元素的化合价代数和为零,钙元素显+2价,氧元素显-2价,CaSO3中硫元素的化合价为+4,反应②的化学方程式是2CaSO3+O2=2CaSO4;(3)分离操作a是将难溶性固体与液体分离,操作是过滤,所需的玻璃仪器有烧杯、玻璃棒和漏斗;(4)生产流程中生成的NaOH溶液在反应物中存在,而且在后续的过程中又产生,可循环利用,节约成本。

【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
查阅资料
a.固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。
b.氯化钙、氯化溶液均呈中性。
(提出问题)
①酒精中是否含有碳元素?
②固体酒精中的氢氧化钠是否变质?
(实验探究)
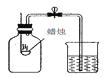
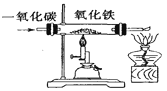
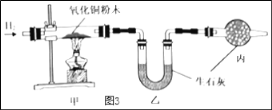
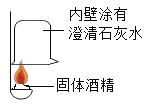
①按右图所示进行实验,发现烧杯内壁有一层白膜,可得出酒精中含有碳元素的结论,理由是_______________。
②取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀是如何形成的:_______________由此说明氢氧化钠已变质。
③为进一步确定氢氧化钠的变质程度,分组进行探究。
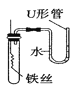
甲组同学取烧杯上层清液于两支试管中,按下图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生______________ |
实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是_______________
他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)乙组实验中加足量氯化钡溶液的目的是_____________
(实验结论]小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。
【题目】K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下。下列说法错误的是( )
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
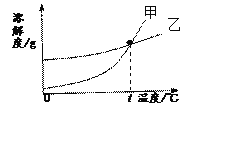
A. t℃在60℃到80℃之间,且甲表示KNO3的溶解度曲线
B. t℃时,甲、乙两种溶液的溶质质量分数不一定相等
C. 把60℃时的105g KNO3饱和液降温至20℃,能析出晶体78.4g
D. 两种饱和液从80℃降温到20℃,析出晶体的质量(不含结晶水)无法比较