题目内容
【题目】过氧化钠(Na2O2)可作为供氧剂。兴趣小组同学查阅资料发现过氧化钠有如下性质:
a.与二氧化碳反应生成碳酸钠和氧气;b.和水反应生成氢氧化钠和氧气。
实验目的:验证过氧化钠能与二氧化碳反应,并检验生成的碳酸钠和氧气。兴趣小组用如下装置进行实验,其中A处为CO2发生装置。

①A处二氧化碳气体的发生装置。下列是实验室常用的仪器:

其中仪器c的名称是______。组装二氧化碳发生装置时,仪器组合错误的是______ (选填编号)。
甲 acfh 乙 bcfg 丙 adfh 丁 bdeg
②A处装置中若反应消耗了0.1molCaCO3,则生成的CO2的质量是多少g?(请根据化学方程式列式计算)____________。
③写岀B处过氧化钠与二氧化碳反应的化学方程式____________。
④D中收集氧气的方法称为___________,检验试管中是氧气的方法是________。
⑤有同学认为应増加一个装置使整套实验装置更符合实验目的。请你阐述需要増加的实验装置的作用是_________,以及添加的位置是__________。
⑥若要检验产物碳酸钠,取B中反应后样品进行实验,请完成下表中空白处的实验方法:
实验步骤 | 实验方法 | 现象或结论 |
一 | 加入足量的稀盐酸 | _____________ |
二 | ______________ | 存在碳酸钠 |
【答案】长颈漏斗 丁 4.4g ![]() 排水法 带火星的木条伸入试管内,木条复燃 干燥 在AB装置之间 有气泡生成 将气体导入澄清石灰水中
排水法 带火星的木条伸入试管内,木条复燃 干燥 在AB装置之间 有气泡生成 将气体导入澄清石灰水中
【解析】
①仪器c的名称是:长颈漏斗;
甲:a、锥形瓶:反应容器;c:长颈漏斗:用于添加稀盐酸;f:由于有长颈漏斗,需要双孔塞;h:导管,组装正确,不符合题意;
乙:b:试管:反应容器;c:长颈漏斗:用于添加稀盐酸;f:由于有长颈漏斗,需要双孔塞;g:带止水夹的导管,组装正确,该装置可以控制反应的发生和停止,不符合题意;
丙:a:锥形瓶:反应容器;d:分液漏斗:用于添加稀盐酸;f:由于有分液漏斗,需要双孔塞;h:导管,组装正确,该装置可以控制反应速率,不符合题意;
丁:b:试管:反应容器;d:分液漏斗:用于添加稀盐酸;e:由于有导管和分液漏斗,应用双孔塞,不是单孔塞;g:带止水夹的导管,组装错误,符合题意。
故选丁;
②CaCO3的质量:0.1mol×100g/mol=10g
设生成的CO2的质量是x。

![]()
![]() x=4.4 g
x=4.4 g
答:生成CO2的质量是4.4 g;
③过氧化钠能与二氧化碳反应,生成碳酸钠和氧气,该反应的化学方程式为:![]() ;
;
④D中收集氧气的方法是:排水法;
氧气具有助燃性,能使带火星木条复燃,常用带火星木条检验氧气。检验试管中是氧气的方法是:带火星的木条伸入试管内,木条复燃,说明是氧气;
⑤该实验的目的是:验证过氧化钠能与二氧化碳反应,并检验生成的碳酸钠和氧气,但是碳酸钙与稀盐酸反应生成的二氧化碳中携带着水蒸气,过氧化钠也能与水反应生成氢氧化钠和氧气,也能使带火星的木条复燃,故应在A、B之间增加一个干燥装置,除去水蒸气,故填:干燥、在A、B装置之间;
⑥要检验产物碳酸钠,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,然后验证生成的气体是二氧化碳即可,故加入足量稀盐酸,稀盐酸与碳酸钠反应生成二氧化碳,实验现象为:有气泡产生;将气体通入澄清石灰水,澄清石灰水变浑浊,则存在碳酸钠。

 阅读快车系列答案
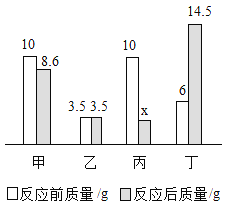
阅读快车系列答案【题目】在密闭容器中有甲、乙、丙、丁四种物质、在一定条件下反应,测得反应前及反应过程中的t1和t2两个时刻各物质的质量如下表所示,其中 a、b、c、d 分别表示相应物质的质量。下列数据不正确的是( )
时间 | 甲 | 乙 | 丙 | 丁 |
反应前 | 70g | 14g | 6g | 10g |
t1 时刻 | a | 11g | c | d |
t2时刻 | 42g | b | 40g | 10g |
A. a=56gB. b=8gC. c=17gD. d=10g
【题目】某实验学校初三兴趣小组利用如下装置(部分固定装置已略去)。制备氮化钙,并探究其化学式
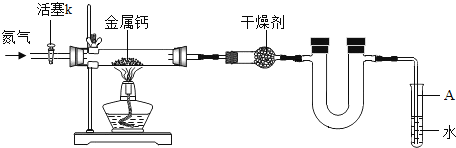
(1)制备氮化钙的操作步骤有:①打开活塞k并通入N2;②点燃酒精灯,进行反应;③反应结束后,_____;④拆除装置,取出产物。
(2)干燥剂的作用是_____;
(3)装置中U型管的作用是_____。
(4)数据记录如下:
空硬玻璃管质量m0/g | 硬玻璃管与钙的质量m1/g | 硬玻璃管与产物的质量m2/g |
114.8 | 120.8 | 122.2 |
①计算得到化学式(实验式)CaxN2,其中x=____。
②若通入的N2中混有少量O2,则测得氮元素质量会_____(填写“偏大”、“偏小”、“不变”,下同),其依据是_____,如上计算得到的x会____。