题目内容
【题目】NaCl、KNO3、Ca(OH)2三种物质的溶解度曲线如图1与图2所示.请回答:
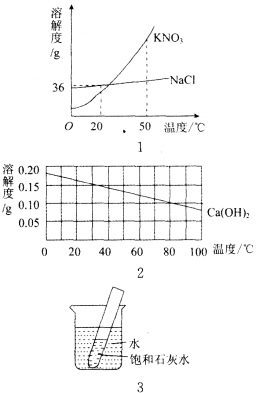
(1)由图1可知,20℃时氯化钠的溶解度为________g;50℃时氯化钠的溶解度(填“>”或“<”)________硝酸钾的溶解度.
(2)欲对含有少量硝酸钾的氯化钠固体进行提纯,可以使用的结晶方法是________.
(3)如图3所示,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体后,石灰水变浑浊,结合图2分析其原因是________________________.
【答案】(1)36 < (2)蒸发结晶
(3)氢氧化钠固体溶于水放热,而氢氧化钙的溶解度随温度的升高而逐渐减小,所以结晶析出
【解析】(1)根据溶解度曲线可知,20℃时氯化钠的溶解度为36g,50℃时氯化钠的溶解度小于硝酸钾的溶解度.(2)由于硝酸钾的溶解度受温度变化影响较大,而氯化钠的溶解度受温度变化影响较小,因此,将两种固体的混合物溶于水,然后蒸发结晶即可得到氯化钠固体.(3)氢氧化钠固体溶于水放出热量,由于氢氧化钙的溶解度随温度升高而减小,因此,饱和石灰水中会析出晶体,导致石灰水变浑浊.

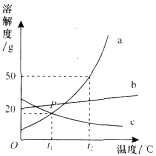
【题目】20℃时,取相同质量的a、b、c三种物质的饱和溶液分别置于三个烧杯中,再分别向其中加入相同质量的相应固体溶质,将温度升高到40℃,固体的溶解情况如图A所示.图B为a、b、c三种物质的溶解度曲线.请仔细阅读图A和图B回答下列问题:

(1)三种物质的溶解度关系为b>a>c时的温度为t℃,则t的取值范围是________.
(2)烧杯甲里是________物质的溶液,烧杯乙里是________物质的溶液.
(3)40℃时,烧杯________里的溶液中溶剂最少.
(4)各种状态下,各烧杯(甲、乙、丙)里的溶液中溶质质量分数的比较一定正确的是________.
A.甲(状态2)>甲(状态1) |
B.乙(状态1)>甲(状态3) |
C.甲(状态1)=乙(状态2) |
D.乙(状态3)>丙(状态3) |