题目内容
【题目】甲、乙两个实验小组分别进行“Na2CO3和NaCl混合物中含量测定 ”的实验
(1)甲组的方法是:用质量分数为10%的盐酸滴入到10g的混合物中,根据消耗盐酸溶液的体积来测定碳酸钠的含量。在实验过程中除盐酸、样品与水以外,判断反应是否完全必须用到的试剂是 ,现有某实验小组测得消耗盐酸(密度约为1g/ml)的体积是3.65ml,则该混合物中Na2CO3的质量分数 ;
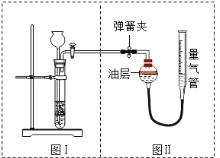
(2)乙组的方法是:将样品与稀盐酸反应,测定反应后生成CO2的体积,经换算并计算出样品中Na2CO3的质量。用上图装置测定产生的CO2的体积。使反应前后油层上方气体压强与外界大气压相同的操作方法是 ;
(3)请你再设计一个与甲、乙操作不同的试验方法,测定混合物中Na2CO3的含量。设计方法是 。
【答案】(1)指示剂 ,5.3% (2)打开弹簧夹 ;移动量气管,使油层与量气管的液面处于同一水平面
(3)取一定量的混合物溶解后加入足量的CaCl2,然后过滤、洗涤、烘干、称量碳酸钙的质量,由碳酸钙的质量算出Na2CO3的质量
【解析】
试题分析:用质量分数为10%的盐酸滴入到10g的混合物中,根据消耗盐酸溶液的体积来测定碳酸钠的含量。在实验过程中除盐酸、样品与水以外,判断反应是否完全必须用到的试剂是指示剂;设现有某实验小组测得消耗盐酸(密度约为1g/ml)的体积是36.5ml,则该混合物中Na2CO3质量是X,
Na2CO3+2HCL=2NaCl+CO2↑+H2O
106 73
X 3.65 ml×1 g/ml 求得X=0.53克 所以该混合物中Na2CO3的质量分数=0.53克/10克×100%=5.3%,使反应前后油层上方气体压强与外界大气压相同的操作方法是打开弹簧夹 ;移动量气管,使油层与量气管的液面处于同一水平面;依据测量原理可以知道碳酸钠可以通过转化为二氧化碳的测量,同时也可以通过转化为碳酸盐的沉淀来进行测量。故依据复分解反应的条件可以得到该物质是氯化钙,会得到碳酸钙的沉淀,通过测量得到的氯化钙的质量来进行计算。