题目内容
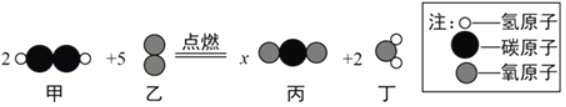
【题目】如图为某化工企业生产流程示意图,下列说法正确的是( )

A. ③中氩气(Ar)作反应物
B. 钛酸亚铁是铁和钛的合金
C. ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1
D. ①中反应为:2FeTiO3+6C+7Cl2![]() 2X+2TiCl4+6CO,则X为FeCl2
2X+2TiCl4+6CO,则X为FeCl2
【答案】C
【解析】
A.氩气是一种稀有气体,化学性质稳定,在反应过程中作保护气,故错误;
B.钛酸亚铁是由铁、钛、氧三种元素组成的化合物,不是合金,故错误;
C.根据从化学方程式:
![]()
由此可知一氧化碳和氢气的质量比是:28:4=7:1,故正确;
D.根据质量守恒定律,在反应前后各元素原子的个数不变。从2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO看钛原子、氧原子、碳原子反应前后除物质x外个数已经相等,故x中无钛原子、氧原子、碳原子。铁反应前共有2个,反应后只有x有,所以2x中有2个,从而x中有1个;氯原子反应前有14个,反应后x除外有8个,所以2x中有6个,因此x中有3个,因此x的化学式是FeCl3,故错误。
故选:C。

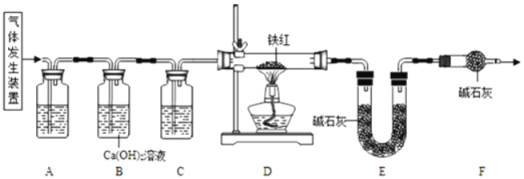
【题目】学习了酸与碱的化学性质后,兴趣小组的同学利用实验室的一瓶氢氧化钠溶液进行如下探究。
探究Ⅰ(提出问题) 该氢氧化钠溶液是否已经变质?
氢氧化钠露置于空气中变质的反应方程式_________,___(填“是”或“不是”)复分解反应。
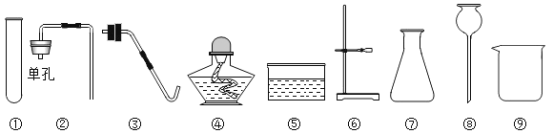
(实验探究)
实验操作 | 实验现象 | 实验结论 |
方法1:取样,滴加足量的______, | 无气体产生 | 氢氧化钠溶液没有变质 |
方法2:取样,滴加氢氧化钙溶液 |
(实验结论)氢氧化钠溶液没有变质。
探究Ⅱ(提出问题) 中和反应过程中是否有能量变化?
(实验探究)
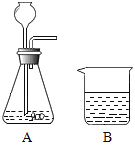
甲同学:取适量该氢氧化钠溶液,滴加1~2滴酚酞,在溶液中插入温度计,再逐滴加入稀盐酸,边滴加边搅拌,测得温度变化情况如图所示。
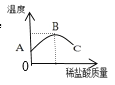
①写出该反应的化学方程式___________,实验中搅拌的目的是____________;
②从图像可知,中和反应是____过程;请解释BC段的成因__________。
乙同学:取少量氢氧化钠固体与稀盐酸反应进行实验,得出了同样的结论。小华同学认为,乙同学的结论不可信,你认为她的理由是___________。