题目内容
【题目】学习了酸与碱的化学性质后,兴趣小组的同学利用实验室的一瓶氢氧化钠溶液进行如下探究。
探究Ⅰ(提出问题) 该氢氧化钠溶液是否已经变质?
氢氧化钠露置于空气中变质的反应方程式_________,___(填“是”或“不是”)复分解反应。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
方法1:取样,滴加足量的______, | 无气体产生 | 氢氧化钠溶液没有变质 |
方法2:取样,滴加氢氧化钙溶液 |
(实验结论)氢氧化钠溶液没有变质。
探究Ⅱ(提出问题) 中和反应过程中是否有能量变化?
(实验探究)
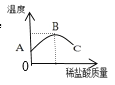
甲同学:取适量该氢氧化钠溶液,滴加1~2滴酚酞,在溶液中插入温度计,再逐滴加入稀盐酸,边滴加边搅拌,测得温度变化情况如图所示。
①写出该反应的化学方程式___________,实验中搅拌的目的是____________;
②从图像可知,中和反应是____过程;请解释BC段的成因__________。
乙同学:取少量氢氧化钠固体与稀盐酸反应进行实验,得出了同样的结论。小华同学认为,乙同学的结论不可信,你认为她的理由是___________。
【答案】2NaOH+CO2═Na2CO3+H2O 不是 稀盐酸 NaOH+HCl═NaCl+H2O 使稀盐酸和氢氧化钠溶液充分反应 放热 完全反应后不再放热,逐渐冷却 氢氧化钠固体溶于水放热
【解析】
氢氧化钠溶于水放热,能和二氧化碳反应生成碳酸钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠。
探究Ⅰ:氢氧化钠露置于空气中变质,是因为氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O,不是复分解反应;
[实验探究]方法1:取样,滴加足量的稀盐酸,不产生气泡,说明溶液中不含有碳酸钠;
方法2:取样,滴加氢氧化钙溶液,不产生沉淀,说明溶液中不含有碳酸钠;
探究Ⅱ[实验探究]甲同学:①氢氧化钠和稀盐酸反应生成氯化钠和水,该反应的化学方程式为:NaOH+HCl═NaCl+H2O,实验中搅拌的目的是使稀盐酸和氢氧化钠溶液充分反应;
②从图象可知,随着反应进行,温度升高,说明中和反应是放热过程;BC段温度下降原因:完全反应后不再放热,逐渐冷却;乙同学:乙同学的结论不可信,她的理由是氢氧化钠固体溶于水放热,影响对实验结果的判断。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】对比实验是化学研究中经常采用的方法。化学兴趣小组的同学在研究CO2通入NaOH溶液是否发生了反应,设计了下列二组实验。请和化学兴趣小组的同学一起探究并回答问题:
(设计与实验)
实验 序号 | 实验步骤一 | 实验步骤二 | 实验 序号 | 实验步骤一 | 实验步骤二 |
实验I |
|
| 实验II |
|
|
(探究与结论)
(1)实验I中步骤一看不到明显现象,步骤二产生的现象是____________________。(2)实验Ⅱ中步骤二看到有白色沉淀析出,则发生反应的化学方程式是__________。
(3)在实验Ⅱ的步骤一中CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是____________________。
(拓展延伸)现有下列信息:
资料卡片一
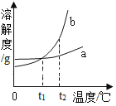
20℃NaOH、Na2CO3在水中的溶解度
物质 溶解度(S)/g
NaOH 109
Na2CO3 21.8
资料卡片二
20℃NaOH、Na2CO3在乙醇中的溶解度
物质 溶解度(S)/g
NaOH 17.3
Na2CO3 <0.01
请你和化学兴趣小组的同学一起利用以上料信息再设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。
实验Ⅲ的操作为:_____________________________。
看到的现象是_________________________________。