��Ŀ����
����Ŀ�����������ʵ��װ��ͼ�ش��й����⡣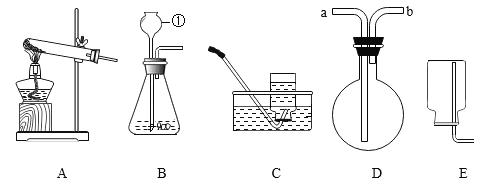
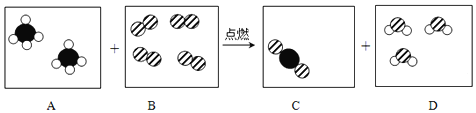
(1)д��������������ƣ���_________
(2)ʵ����ѡ��A��Bװ�ö����Ʊ���������________ (�ѧʽ)����Aװ����ȡ������Ļ�ѧ��Ӧ����ʽΪ___________________________
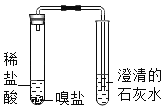
(3)ʵ������ȡ����������̼ʱ����ѡ�÷���װ��Ϊ_________����ѧ��Ӧ����ʽΪ__________��ѡ��Dװ���ռ�CO2������װ��Ӧ����_________�˿�(��a��b)��
(4)ij��ȤС������ѹ���������������ֻ�ʵ����̽��CO2�ֱ���ˮ��ʯ��ˮ������������Һ�ķ�Ӧ�����ʵ������������£�
a.���ݻ�Ϊ250mL��Dװ�ü�����ƿCO2���á�
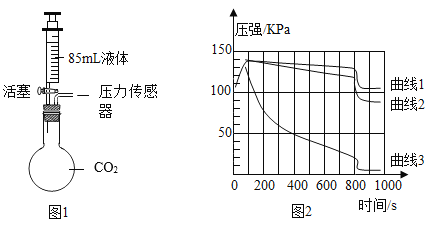
b.��������ע�����ֱ�װ��85mL����Һ�壺ˮ��0.16%���ͳ���ʯ��ˮ��40%���������ܰ�ͼ1���Ӻ�װ�ú�ѹ����������c.��λͬѧͬʱѸ�ٽ�ע������Һ��ȫ��ע�������ƿ�У��رջ�����һ��ʱ���ͬʱ����ƿ�������������ֻ�ʵ��ⶨ��ƿ��ѹǿ��ʱ��仯��������ͼ2��ʾ��
��ش�
������1��ʾ��_________������ƿ��ѹǿ�仯��
������3��ʾ��_________������ƿ��ѹǿ�仯��
������2������3����ϴ��ԭ����_________
��800s����ѹ���ٱ�С�IJ�����_________
���𰸡�����©�� O2 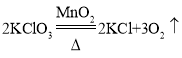 B CaCO3+2HCl=CaCl2+H2O+CO2�� a H2O NaOH ���ͳ���ʯ��ˮŨ�Ƚ�С��40% NaOHŨ�Ƚϴ�����CO2�϶� ����ƿ
B CaCO3+2HCl=CaCl2+H2O+CO2�� a H2O NaOH ���ͳ���ʯ��ˮŨ�Ƚ�С��40% NaOHŨ�Ƚϴ�����CO2�϶� ����ƿ
��������
(1)���������ƣ��ٳ���©����
(2)ʵ����ѡ��A�������װ�û�B�̡�Һ����װ�ö����Ʊ���������������O2����Aװ�õ��Թ���û���������������������̻�ϼ��Ȳ����Ȼ��غ������Ļ�ѧ��Ӧ����ʽΪ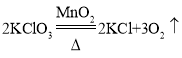 ��
��
(3)ʵ������ȡ����������̼ʱ����ѡ�ù̡�Һ����װ��ΪB������ʯ��ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�Ļ�ѧ��Ӧ����ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2����������̼���ܶȴ��ڿ�������ѡ��Dװ���ռ�CO2������Ӧ�á����ܽ����̹ܳ���������װ��Ӧ����a�˿ڡ�
(4) ������1��ʾ��ˮ������ƿ��ѹǿ�仯����Ϊˮ���������̼��Ӧ����̼�ᣬ��̼��ȶ�����ֽ����������̼���壬ѹǿ���н�С��
������3��ʾ������������Һ������ƿ��ѹǿ�仯����Ϊ����������Һ���������̼���巴Ӧ����̼������Һ��������ȫ�����գ�ѹǿ��С���ԡ�
������2������3����ϴ��ԭ���ǣ����ͳ���ʯ��ˮŨ�Ƚ�С�����յĶ�����̼�����٣�40% NaOHŨ�Ƚϴ�����CO2�϶ࣻ����ѹǿ���Բ�ͬ��
��800s����ѹ���ٱ�С�IJ����ǣ�����ƿ���Ƕ�����̼��Һ�������Ӵ�����ַ�Ӧ��

����Ŀ����������������Ե���Ա���ٻָ���ʶ���õ������Ρ���ͬѧ�Ƕԡ����Ρ������˺��棬������ɷֽ�������̽����
���������ϣ�����������һ���������ʺ����ϣ�����������̽���е��κη�Ӧ����ɣ����ͷų���ζ���壬�����������ǿ�ҵĴ̼����ã������������Σ��������
���Ȼ���ϡ��Һ��̼�����ϡ��Һ��������Ӧ��
�������������ữ����������李�
��������⣩����������������ʲô��
��ʵ��̽������д���пո�
ʵ�� | С����ʵ�� | СӢ��ʵ�� | |
���� |
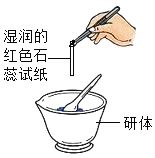
������_____����һ�����ʣ������ĥ |
|
|
���� | �ŵ���Ũ�Ҵ̼�����ζ����ֽ���� | _____ | _____ |
���� | �����к���NH4+ | �����к�CO32�� | ȷ����С����ʵ����� |
֤������������������̼��� | |||
�����ɣ�СӢ��ΪС����ʵ����۲��Ͻ���СӢͨ������һ��ʵ�飨�������ϱ���������ȷ����С���Ľ��ۡ�СӢ��ʵ��Ŀ�����ų������к���_____���ӵĿ����ԡ�
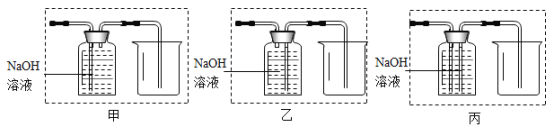
������̽����ͬѧ��������ͼװ�ý�һ���ⶨ������̼��淋�����������
��Ӧԭ������NH4��2CO3+2NaOH![]() X+2NH3��+2H2O������X�Ļ�ѧʽΪ_____��
X+2NH3��+2H2O������X�Ļ�ѧʽΪ_____��
�����ݼ�¼��ʵ���ȡ��Ʒ����Ϊm1����Ӧǰ��װ���������ƹ�������θ���ܵ��������ֱ�Ϊm2��m3����Ӧǰ���ձ����ձ�����Һ���������ֱ�Ϊm4��m5��
�����ݴ�����ͨ��������ݼ����������̼��淋�����������
����˼�����ۣ����ڸ�ʵ���˵����ȷ����_____������ţ�˫ѡ����
A��������̼��淋�������������ʽΪ��![]() ��100%
��100%
B������©�����������������ͬʱ��ֹ����
C��������Ũ�������ϡ����
D��ֹͣ���Ⱥ�Ҫͨ��һ��ʱ�����������ⶨ�����ƫС

����Ŀ��ij��ȤС�����������������̵Ļ������ȡ�������Թ��й����������ʱ��仯�����ݼ��±�����ȡ������ʣ�����������ˮ����ܽ���ˣ����ն���������
�壬���õ��Ȼ�����Һ200g��
����ʱ��/min | 0 | t1 | t2 | t3 |
��������/g | 26.0 | 23.4 | 16.4 | 16.4 |
����㣺
��1�����Ƶ�����______g��
��2�������Ȼ�����Һ�����ʵ�����������______
����Ŀ��ʯ��ʯ����ʡ����Ҫ���֮һ��ѧУ�о���ѧϰС��Ϊ�˲ⶨ���ؿ�ɽʯ��ʯ��̼��Ƶ�����������ȡ����һЩ��ʯ��Ʒ����ȡϡ����200g��ƽ���ֳ�4�ݽ���ʵ�飬������±���
ʵ�� | 1 | 2 | 3 | 4 |
������Ʒ������/g | 5 | 10 | 15 | 20 |
���ɵ�CO2����/g | 1.76 | 3.52 | 4.4 | m |
��1���ļ��η�Ӧ��̼�����ʣ�ࣿ_______
��2���ϱ���m��ֵΪ��_______
��3���Լ�������ʯ��ʯ��̼��Ƶ�����������_______