题目内容
【题目】蚊虫叮咬时能在人体皮肤内分泌蚁酸,让人痛庠不止。某课外小组同学决定对蚁酸进行探究。
(查阅资料) 蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;蚁酸在一定条件下会分解成两种氧化物。
(提出问题)蚁酸的成分是什么?它有什么性质?
(1)小明同学根据蚁酸中含有氢元素,推测出分解的生成物中含有 ______ ;
(2)另一种生成物是气体,小刚提出两种猜想:
猜想①:该气体是 ______ ;
猜想②:该气体是一氧化碳。
(实验探究)
(3)向盛有蚁酸溶液的试管中滴加紫色石蕊溶液,观察到溶液变 ______ 。
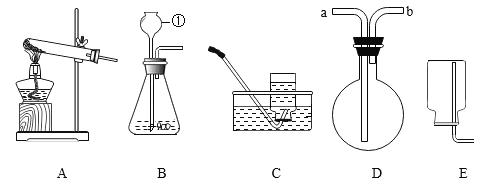
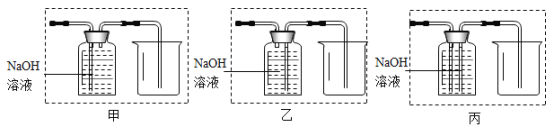
(4)将蚁酸分解产生的气体通过如下图所示的装置(铁架台已略去),观察现象。

I.实验时装置A中无明显变化,则猜想① ______ (选填”成立”或“不成立”)。
Ⅱ.实验时装置C和D中均有明显现象,由此得出猜想②成立,则C中的现象是 ______ ,反应的化学方程式为 _______________。
(评价反思)
(5)从环保角度看,该装置存在的缺陷是 ___________。
(6)兴趣小组的同学设计了下图所示的甲、乙、丙三个虚线框内的药品及装置,准备连接在C装置后来达到收集纯争的CO的目的,你认为选择哪个装置最好? ______ ;反应的化学方程式为_______。
(拓展延伸)
(7)小组同学利用pH试纸比较蚁酸、盐酸的酸碱性强弱,实验中你认为要控制的变量是______。
(8)蚊虫叮咬后,在叮咬处涂抹一些物质可以减轻痛痒,下列物质中不能擦拭的是______。
A 稀氨水 B 氢氧化钠溶液 C 稀醋酸 D 肥皂水
(9)实验中,测定蚁酸的成分时,称量反应前后相关物质的质量,数据如下表:
反应前 | 充分反应后 |
玻璃管和固体物质的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
则:实验取用氧化铜粉末的质量为 ______ g。
【答案】H2O(或水 ) CO2 (或二氧化碳) 红(或红色) 不成立 黑色粉末变红色 CO+ CuO ![]() Cu + CO2 未设置一氧化碳处理装置(或缺少尾气处理装置或没有对尾气进行处理) 丙 2NaOH+CO2=Na2CO3+H2O 蚁酸、盐酸的质量分数 (或蚁酸、盐酸的浓度) B、C 6
Cu + CO2 未设置一氧化碳处理装置(或缺少尾气处理装置或没有对尾气进行处理) 丙 2NaOH+CO2=Na2CO3+H2O 蚁酸、盐酸的质量分数 (或蚁酸、盐酸的浓度) B、C 6
【解析】
[提出问题]
(1)反应前后元素种类不变,乙酸分解生成两种氧化物,小明同学根据蚁酸中含有氢元素,推测出分解的生成物中含有水,故填:H2O(水)。
(2)另一种生成物是气体,是碳的氧化物,可能是一氧化碳也可能是二氧化碳,故填:CO2(二氧化碳)。
[实验探究]
(3)紫色石蕊试液遇酸变红,故填:红。
(4)I.实验时装置澄清石灰中无明显变化说明不含二氧化碳,则猜想① 不成立故填:不成立。
Ⅱ.猜想②成立则气体为一氧化碳,一氧化碳还原氧化铜生成铜和二氧化碳,黑色固体变为红色,反应的化学方程式为CO+ CuO![]() Cu+CO2,故填:黑色粉末变红色;CO+CuO
Cu+CO2,故填:黑色粉末变红色;CO+CuO ![]() Cu+CO2。
Cu+CO2。
[评价反思]
(5)从环保角度看,该装置存在的缺陷是缺少尾气处理装置,一氧化碳有毒会污染环境,故填:未设置一氧化碳处理装置(或缺少尾气处理装置或没有对尾气进行处理)。
(6)连接C装置后来收集纯争的CO的目的,选择丙装置最好,长管进可以使氢氧化钠充分吸收二氧化碳;一氧化碳密度比水小,排水法收集一氧化碳,液体从另一长管排出,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O ,故填:丙;2NaOH+CO2=Na2CO3+H2O。
[拓展延伸]
(7)小组同学利用pH试纸比较蚁酸、盐酸的酸碱性强弱,实验中你认为要控制的变量是蚁酸、盐酸的质量分数 (或蚁酸、盐酸的浓度),故填:蚁酸、盐酸的质量分数 (或蚁酸、盐酸的浓度)。
(8)蚊虫叮咬后,会分泌蚁酸,在叮咬处涂抹一些碱性物质可以减轻痛痒,不能擦拭的是氢氧化钠溶液,氢氧化钠有强烈腐蚀性,以及稀醋酸,稀醋酸显酸性,可以涂抹的是下稀氨水和肥皂水,都是显碱性的,可以减轻痛痒,故选:BC。
(9)反应前后固体质量较少为37.3g-36.1g=1.2g设氧化铜质量为x。

故填:6。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】压强为101kPa下,硝酸钾和氨气在不同温度下的溶解度如下表。下列说法正确的是
温度/℃ | 10 | 20 | 30 | 60 | |
溶解度/g | KNO3 | 20.9 | 31.6 | 45.8 | 110 |
NH3 | 70 | 56 | 44.5 | 20 | |
A. 两种物质的溶解度均随温度升高而增大
B. 20℃时, KNO3饱和溶液中溶质的质量分数为31.6%
C. 60℃的KNO3饱和溶液降温至30℃,有晶体析出
D. NH3的溶解度与压强大小无关
【题目】复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个探究实验。
(1)探究1:研究常见物质组成
A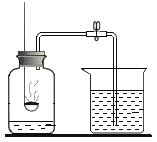 测定空气中的氧气含量 B
测定空气中的氧气含量 B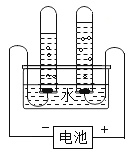 水电解实验 C
水电解实验 C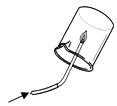 检验甲烷成分
检验甲烷成分
A、B、C都是研究物质组成的实验。从研究方法得知,A实验是利用可燃物消耗瓶内的____,使瓶内压强减小来推测空气里氧气含量的;B实验是通过证明生成物的________来推断水的组成的;而C实验与_____(填实验代号)实验的方法相同。
(2)探究2:研究常见物质性质—氢氧化钠与硫酸是否刚好完全中和
小明用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH﹤7,说明硫酸过量。他决定来验证一下:
实验内容 | 实验现象 | 解释与结论 |
取反应后少量溶液于试管中,________ | ________ | 证明研究结论正确 |
(3)探究3:某同学做“证明鸡蛋壳的主要成分是碳酸盐,并收集纯净的气体”的实验。设计了如下方案进行实验:
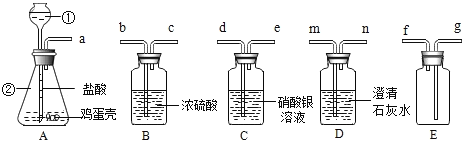
①根据我们所学的知识,你认为A装置和_____装置相连并产生什么现象时就足以说明鸡蛋壳的主要成分是碳酸盐?____;写出该装置中发生反应的化学方程式:__。
②该同学想要收集一瓶纯净的该气体,进一步验证它的性质,连接上述装置的顺序是:(填写各接口字母)____。其中C装置的作用是:______。
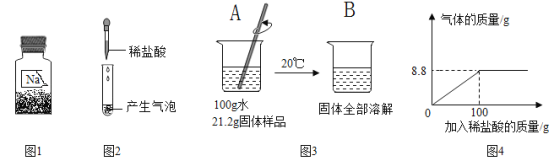
(4)某研究性学习小组在协助老师清理实验储备室时,发现一批存放多年的氢氧化钙。为检验其变质情况,进行了如下探究:取氢氧化钙样品11.4g于锥形瓶中,加入38.6g水,振荡形成悬浊液,放在电子天平上,向锥形瓶中逐滴滴加14.6%的稀盐酸,振荡后读取质量(如图甲所示),实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图乙所示。
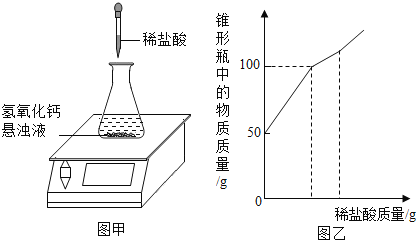
求:11.4g该样品中各成分的质量______。