��Ŀ����
ijʯ�ҳ���һ��ʯ��ʯԭ�ϣ�Ϊ�˲ⶨ��ʯ��ʯ��̼��Ƶ������������������Ҽ���Ա��ȡ12.5g�����ʯ��ʯ��ĩ�������Ĵθ������գ�����û�б仯������ȴ������ʣ������������ظ���������¼�������£�����ʾ��̼����ڸ����·ֽ⣬���������ƺͶ�����̼��

�Լ��㣺
��1����ȫ��Ӧ�����ɶ�����̼ ��
��2��ʯ��ʯ��Ʒ�к�̼��Ƶ���������
��3���������20t����ʯ��ʯ�����Ƶú����ʵ���ʯ�ҵ�������
��1����ȫ��Ӧ�����ɶ�����̼ ��
��2��ʯ��ʯ��Ʒ�к�̼��Ƶ���������
��3���������20t����ʯ��ʯ�����Ƶú����ʵ���ʯ�ҵ�������
��1��4.4
��2����̼��Ƶ���������Ϊx
CaCO3 CaO+CO2��
CaO+CO2��
100 44
x��12.5g 4.4g
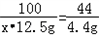 x=80%
x=80%
��ʯ��ʯ��Ʒ�к�̼��Ƶ�����������80%��
��3��20t��80%=16t����ʯ�ҵ�����Ϊy
CaCO3 CaO+CO2��
CaO+CO2��
100 56
16t y
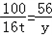 y=8.96t
y=8.96t
�����ʵ���ʯ�ҵ�����=8.96t+��20t��16t��=12.96t
�𣺺����ʵ���ʯ�ҵ�������12.96t��
��2����̼��Ƶ���������Ϊx
CaCO3
 CaO+CO2��
CaO+CO2�� 100 44
x��12.5g 4.4g
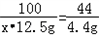 x=80%
x=80% ��ʯ��ʯ��Ʒ�к�̼��Ƶ�����������80%��
��3��20t��80%=16t����ʯ�ҵ�����Ϊy
CaCO3
 CaO+CO2��
CaO+CO2�� 100 56
16t y
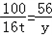 y=8.96t
y=8.96t�����ʵ���ʯ�ҵ�����=8.96t+��20t��16t��=12.96t
�𣺺����ʵ���ʯ�ҵ�������12.96t��

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
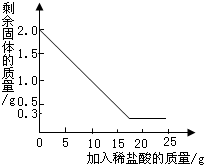 ��ѧ��ȤС���ͬѧ���ۺ�ʵ�����˽��ijʯ�ҳ���һ��ʯ��ʯԭ�ϣ����к��е������Ƕ������裨�������費����ˮ���������ᷴӦ������ʱ�������ֽⷴӦ����Ϊ�˲ⶨ��ʯ��ʯ�Ĵ��ȣ���ȤС��ͬѧȡ��2g����ʯ��ʯ��Ʒ����ȡϡ����20g��4�μ�����Ʒ�н���ʵ�飬������£�
��ѧ��ȤС���ͬѧ���ۺ�ʵ�����˽��ijʯ�ҳ���һ��ʯ��ʯԭ�ϣ����к��е������Ƕ������裨�������費����ˮ���������ᷴӦ������ʱ�������ֽⷴӦ����Ϊ�˲ⶨ��ʯ��ʯ�Ĵ��ȣ���ȤС��ͬѧȡ��2g����ʯ��ʯ��Ʒ����ȡϡ����20g��4�μ�����Ʒ�н���ʵ�飬������£�| ϡ���������/g | ʣ����������/g |
| ��һ�μ���5 | 1.5 |
| �ڶ��μ���5 | 1.0 |
| �������5 | 0.5 |
| ���Ĵμ���5 | 0.3 |
��2��2g��ʯ��ʯ��Ʒ������ϡ���ᷴӦ�������CO2��������
 ��ѧ��ȤС��ͬѧ���ۺ�ʵ������˽��ijʯ�ҳ���һ��ʯ��ʯԭ�ϣ����к��е������Ƕ������裨�������費����ˮ�����������ᷴӦ������ʱ�������ֽⷴӦ����Ϊ�˲ⶨ��ʯ��ʯ�Ĵ��ȣ���ȤС��ͬѧȡ��2g����ʯ��ʯ��Ʒ����ʵ�������е�δ֪��������������ϡ����20g��4�μ��룬��ַ�Ӧ�����ˡ�����Ȳ����������ÿ��ϡ����������ʣ�������������±�������ʵ�����ݻ��Ƶ�ͼ�����ͼ��������һλ��Ч���֣�
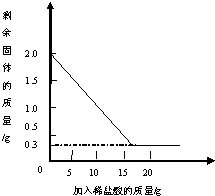
��ѧ��ȤС��ͬѧ���ۺ�ʵ������˽��ijʯ�ҳ���һ��ʯ��ʯԭ�ϣ����к��е������Ƕ������裨�������費����ˮ�����������ᷴӦ������ʱ�������ֽⷴӦ����Ϊ�˲ⶨ��ʯ��ʯ�Ĵ��ȣ���ȤС��ͬѧȡ��2g����ʯ��ʯ��Ʒ����ʵ�������е�δ֪��������������ϡ����20g��4�μ��룬��ַ�Ӧ�����ˡ�����Ȳ����������ÿ��ϡ����������ʣ�������������±�������ʵ�����ݻ��Ƶ�ͼ�����ͼ��������һλ��Ч���֣� ijʯ�ҳ���һ��ʯ��ʯԭ�ϣ����к��е����ʲ������ᷴӦ��Ϊ�˲ⶨ��ʯ��ʯ�Ĵ��ȣ���ȤС���ͬѧȡ��2g����ʯ��ʯ��Ʒ������20gϡ������Ĵμ��룬��ַ�Ӧ�����ˡ�����Ȳ�������ÿ��ϡ����������ʣ�����������ʵ�����ݻ��Ƴ�ͼ����ͼ�������㣺
ijʯ�ҳ���һ��ʯ��ʯԭ�ϣ����к��е����ʲ������ᷴӦ��Ϊ�˲ⶨ��ʯ��ʯ�Ĵ��ȣ���ȤС���ͬѧȡ��2g����ʯ��ʯ��Ʒ������20gϡ������Ĵμ��룬��ַ�Ӧ�����ˡ�����Ȳ�������ÿ��ϡ����������ʣ�����������ʵ�����ݻ��Ƴ�ͼ����ͼ�������㣺