题目内容
【题目】下列是初中化学中的一些常见实验,请回答下列问题:
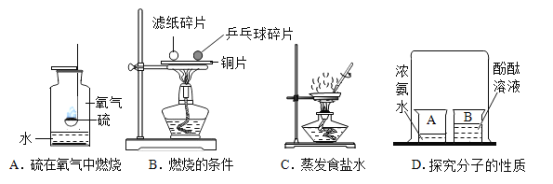
(1)A实验中,为了更好地吸收二氧化硫,可将水替换为_____溶液;(填一种具体物质名称)
(2)B实验中,可以说明燃烧的条件之一是_____;
(3)C实验中,玻璃棒不断搅拌的目的是_____;
(4)D实验中,一段时间后观察到的现象是_____。
【答案】氢氧化钠 温度达到可燃物的着火点 防止局部温度过高,造成液滴飞溅 2中溶液由紫色变成红色
【解析】
二氧化硫能与氢氧化钠反应生成亚硫酸钠和水,浓盐酸具有挥发性,挥发出来的氯化氢气体不断地运动,燃烧条件:物质本身是可燃物,有氧气参与,达到可燃物的着火点。
(1)二氧化硫能与氢氧化钠反应生成亚硫酸钠和水,所以可用氢氧化钠溶液来代替水吸收二氧化硫气体。
(2)实验中,观察到乒乓球碎片先燃烧。,滤纸碎片后燃烧,说明燃烧的条件是温度要达到可燃物的着火点。
(3)蒸发操作中,玻璃棒不断搅拌的目的是防止局部温度过高,造成液滴飞溅。
(4)浓盐酸具有挥发性,挥发出来的氯化氢气体不断地运动,与石蕊试液中的水结合成盐酸,盐酸能使紫色的石蕊试液变红色。

【题目】在一密闭容器里放入四种物质,使其在一定条件下反应,一段时间后,测得数据如下:则下列表述正确的是( )
四种物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 25 | 15 | 1 | 5 |
反应后质量/g | 11 | 未测 | 1 | 22 |
A. 未测值为2B. 丙可能是催化剂
C. 该反应为化合反应D. 甲与乙反应的质量比为![]()
【题目】金属锌与稀硫酸反应生成硫酸锌和氢气,化学课外小组的同学对“锌与硫酸反应快慢的影响因素”进行了探究。
(提出问题)锌与硫酸反应的快慢受哪些因素的影响呢?
(猜想与假设)a.可能与稀硫酸的浓度有关;b.可能与锌的形状有关。
(设计并实验)小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号 | 稀硫酸的浓度(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)锌与稀硫酸反应的化学方程式为_____。
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是_____。
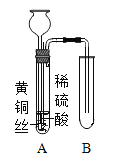
(3)利用如图装置进行实验时,为了较准确的测量氢气的体积,在读取量气管中液面读数的过程中,应注意_____(填字母编号)。
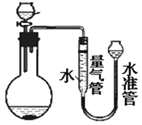
A.读数时视线与凹液面最低处相平。
B.保持水准管静止,待水准管中液面不再上升时再读数。
C.读数前应上下移动水准管,待两管液面相平再读数。
通过上述实验,你得出的结论是硫酸的质量分数越大,反应速率越快。锌与硫酸的接触面积越大,反应速率越快
(4)发生装置中留有氢气,是否会影响实验最终结果_____(填“是”或“否”)。
(5)下表是小组同学第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第4分钟 | 第3分钟 | 第5分钟 | 第6分钟 |
H2的体积 | 3.1mL | 16.7mL | 9.6mL | 11.9mL | 7.6mL | 6.0mL |
解释第二分钟以后变化的原因_____。