题目内容
【题目】(6分)下表是NaCl和KNO3在不同温度时的溶解度,请根据相关信息回答下列问题。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(1)60℃时,在100 g水里溶解_________g KNO3时,溶液才可达到饱和状态。
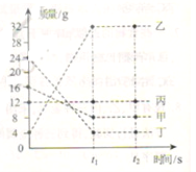
(2)下图为NaCl 和KNO3的溶解度曲线,则表示NaCl的溶解度曲线是_________(填“甲”或“乙”);其中温度t的范围可能在________(填字母序号)。
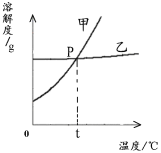
A.10℃~20℃之间 B.20℃~30℃之间
C.30℃~40℃之间 D.40℃~50℃之间
(3)请根据上表或图示总结出一条具有一定规律的结论 。
(4)在0℃时,分别在100 g 水中加入30 g NaCl 和KNO3固体,再加热到60℃时(假设溶剂不损耗),NaCl溶液为______(填“饱和”或“不饱和”)溶液。加热前后,有关两种溶液的说法正确的是_____(填字母序号)。
A.0℃时,两溶液中溶质的质量分数相同
B.60℃时,两溶液中溶质的质量分数相同
C.加热前后,NaCl溶液中溶质的质量分数由小变大
D.加热前后,KNO3溶液中溶质的质量分数不变
【答案】(1)110 (2)乙 B (3)硝酸钾的溶解度随温度的升高,逐渐增大;
(4)不饱和 B
【解析】
试题分析:(1)由表中数据可知60℃时,硝酸钾的溶解度为110g,因此该温度下在100g水里溶解 110gKNO3时,溶液才可达到饱和状态.
(2)0℃时氯化钠的溶解度大于硝酸钾的溶解度,因此乙曲线是氯化钠溶解度曲线,由表中数据可知在20℃-30℃之间
氯化钠的溶解度在36g~36.3g之间,硝酸钾的溶解度在31.6g~45.8g之间,两物质有相同的溶解度.
(3)由表格数据或溶解度曲线可以看出硝酸钾的溶解度受温度影响较大,氯化钠溶解度受温度影响较小.
(4)0℃时,氯化钠的溶解度为35.7g,在此温度下在100g水中加入30gNaCl得到的是不饱和溶液,而0℃时KNO3固体的溶解度为13.3g,此温度下,100g水中加入30g硝酸钾得到的是饱和溶液,当加热到60℃时,氯化钠的溶解度为37.3g,此时仍然是不饱和溶液,而硝酸钾在60℃时的溶解度为110g,此温度下是硝酸钾的不饱和溶液.
A、由上述分析可知0℃时两溶液中溶质的质量分数不相同,氯化钠溶液的溶质质量分数大于硝酸钾的溶质质量分数.故A错误;
B.60℃时两溶液都是不饱和溶液,溶质的质量分数相同,正确;
C.加热前后,NaCl溶液中溶质的质量分数不变,因为加热前后都是不饱和溶液,故C错误
D.加热前后,KNO3溶液中溶质的质量分数应由小变大,因为加热前是饱和溶液且有固体剩余,加热后是不饱和溶液,固体全部溶解,故D错误;

【题目】(15分)某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【查阅资料】
①生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质(不与酸反应).
②生产原理反应:NaCl+ NH3 + CO2 + H2O= NaHCO3↓+ NH4Cl,分离得晶体B,并使其充分受热,可分解制得纯碱,同时得到二氧化碳和水.
③氯化铵分解的化学方程式是NH4Cl △ NH3↑+HCl↑.
④部分生产流程如下图所示:
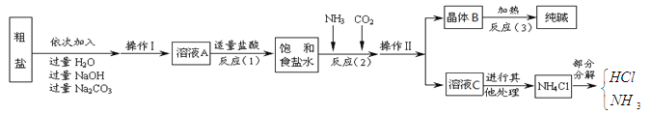
【问题讨论】
(1)①溶液A中的溶质有NaCl和 、 ,
②操作Ⅱ的名称为 .
③流程中Na2CO3溶液的作用是除去粗盐中的 .
④写出加入NaOH溶液与MgCl2反应的化学方程式 .
⑤晶体B受热分解的化学方程式为 .
(2)上述生产流程中可循环使用的是 (填序号).
A.NaOH B.NH3 C.HCl D.CO2
【组成探究一】
(3)设计实验检验纯碱样品中是否混有晶体B,请完成下表
选择的装置 | 实验现象 | 实验结论 |
选择的装置(填序号) | 实验现象 | 实验结论 |
样品不含晶体B |
【组成探究二】
(4)取纯碱样品加水溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.产生沉淀的方程式为 ,由此确定纯碱样品含有杂质NaCl.
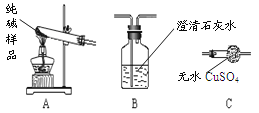
【组成探究三】
(5)同学们为了测定该纯碱样品的纯度,设计了如下实验:
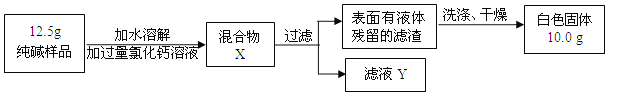
①判断加入氯化钙溶液是否过量的方法是 ,然后观察现象判断.
②判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观察现象判断.
A.氯化钡溶液 B.硝酸银溶液 C.碳酸钠溶液 D.稀盐酸
③根据实验数据,计算样品中碳酸钠的质量分数是多少?(写出计算过程.3分)