题目内容
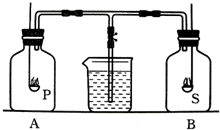 某学习研究小组为探究不同可燃物对测定空气中氧气体积分数实验结果的影响,设计了如右图所示的实验装置.
某学习研究小组为探究不同可燃物对测定空气中氧气体积分数实验结果的影响,设计了如右图所示的实验装置.已知,A、B两只集气瓶中都充满了实验时室温状态下的空气,塞紧瓶塞后气密性良好.燃烧匙中分别盛有过量的红磷和硫,在瓶中点燃并充分燃烧后,冷却至室温.
(1)A瓶中红磷燃烧的化学方程式为
4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
;
| ||
(2)B瓶中硫在燃烧时能观察到的现象为
硫燃烧产生了淡蓝色的火焰
硫燃烧产生了淡蓝色的火焰
;(3)小组成员打开烧杯中导管上的止水夹后,观察到A、B两瓶中都迅速有水被倒吸,且倒吸入瓶中的水的体积相同,都远未达到五分之一体积,实验失败.经过一番分析研究,小组成员们发现原来问题出在实验装置上,只需对该装置做一个改动就能达成原有的实验目的,你知道这个改动是什么吗?
将三通导气管去掉,分别连接导气管插入水中
将三通导气管去掉,分别连接导气管插入水中
.(4)完善实验装置后,该小组成员再次进行了实验,此时可观察到
A
A
瓶中立即有约五分之一体积的水被倒吸,另一瓶中没有水被倒吸.由此可知,测定空气中氧气体积分数时可燃物应选择红磷
红磷
(填“红磷”或“硫”).(5)列式计算:若某一反应中需消耗氧气0.01mol,则至少需要红磷是多少摩尔?
分析:(1)红磷燃烧生成了五氧化二磷,根据反应写出反应的方程式;
(2)根据硫在空气中燃烧的现象分析回答;
(3)根据装置的特点分析,当打来止水夹时,A、B集气瓶是相通的,据此分析改动的措施.
(4)根据测定空气中氧气体积分数的原理分析现象和选择的物质.
(5)根据红磷燃烧的反应方程式计算.
(2)根据硫在空气中燃烧的现象分析回答;
(3)根据装置的特点分析,当打来止水夹时,A、B集气瓶是相通的,据此分析改动的措施.
(4)根据测定空气中氧气体积分数的原理分析现象和选择的物质.
(5)根据红磷燃烧的反应方程式计算.
解答:解:(1)红磷燃烧生成了五氧化二磷,反应的方程式是:4P+5O2
2P2O5;
(2)B瓶中硫在燃烧时能观察到的现象为:硫燃烧产生了淡蓝色的火焰;
(3)由实验的装置可知,A瓶内由于红磷燃烧生成五氧化二磷固体,消耗了氧气,压强减小.B瓶内硫燃烧生了二氧化硫气体,压强不变.当打来止水夹时,A、B集气瓶是相通的.所以,A、B两瓶中都迅速有水被倒吸,且倒吸入瓶中的水的体积相同,都远未达到五分之一体积,实验失败.由此可知,改进的措施是:将三通导气管去掉,分别连接导气管插入水中.
(4)由上述分析可知,完善实验装置后,该小组成员再次进行了实验,此时可观察到A瓶中立即有约五分之一体积的水被倒吸,另一瓶中没有水被倒吸.由此可知,测定空气中氧气体积分数时可燃物应选择红磷.
(5)设至少需要红磷物质的量为x
4P+5O2
2P2O5;
4 5
x 0.01mol
=
解得:x=0.008mol
故答为:(1)4P+5O2
2P2O5;(2)硫燃烧产生了淡蓝色的火焰;(3)将三通导气管去掉,分别连接导气管插入水中;(4)A,红磷;(5)至少需要红磷是0.008摩尔.
| ||
(2)B瓶中硫在燃烧时能观察到的现象为:硫燃烧产生了淡蓝色的火焰;
(3)由实验的装置可知,A瓶内由于红磷燃烧生成五氧化二磷固体,消耗了氧气,压强减小.B瓶内硫燃烧生了二氧化硫气体,压强不变.当打来止水夹时,A、B集气瓶是相通的.所以,A、B两瓶中都迅速有水被倒吸,且倒吸入瓶中的水的体积相同,都远未达到五分之一体积,实验失败.由此可知,改进的措施是:将三通导气管去掉,分别连接导气管插入水中.
(4)由上述分析可知,完善实验装置后,该小组成员再次进行了实验,此时可观察到A瓶中立即有约五分之一体积的水被倒吸,另一瓶中没有水被倒吸.由此可知,测定空气中氧气体积分数时可燃物应选择红磷.
(5)设至少需要红磷物质的量为x
4P+5O2
| ||
4 5
x 0.01mol
| 4 |
| 5 |
| x |
| 0.01mol |
故答为:(1)4P+5O2
| ||
点评:本题主要考查红磷燃烧的方法测定空气中氧气含量实验的原理、操作、现象、结论、注意事项等问题,难度稍大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


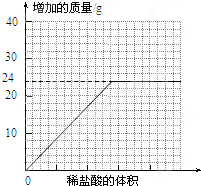
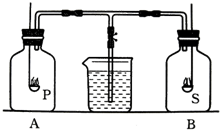 某学习研究小组为探究不同可燃物对测定空气中氧气体积分数实验结果的影响,设计了如右图所示的实验装置.
某学习研究小组为探究不同可燃物对测定空气中氧气体积分数实验结果的影响,设计了如右图所示的实验装置.