题目内容
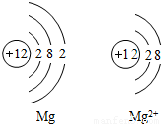
Mg和Mg2+属于________种元素,因为它们的________;S和S2-属于________种粒子,因为它们的________;Na和Na+的化学性质________,因为它们的________;Fe2+和Fe3+的相对原子质量________,因为它们的________.
同种 质子数相同 两 电性 不同 最外层电子数不同 相同 质量都主要集中在原子核上
分析:根据同种元素质子数相同,最外层电子数决定了微粒的化学性质以及原子质量主要集中在原子核上分析解答;
解答:由于Mg和Mg2+的核内质子数相同,所以两者属于同种元素,S和S2-所带电性不同所以两者属于不同的粒子,由于最外层电子数决定了元素的化学性质,所以由于Na和Na+的最外层电子数分别是1和8,故其化学性质一定不同,原子的质量主要集中在原子核上,而电子的质量很小可以忽略不计,因此Fe2+和Fe3+的原子质量几乎无差别(两者原子核无差别核外电子数不同),所以两者的相对原子质量相同;
故答案为:同种;质子数相同;两种;电性;不同;最外层电子数不同;相同;原子的质量主要集中在原子核上;
点评:此题考查了有关元素的基本概念以及元素的化学性质取决于最外层电子数等知识,考查学生基础知识的掌握能力,难度较小.
分析:根据同种元素质子数相同,最外层电子数决定了微粒的化学性质以及原子质量主要集中在原子核上分析解答;
解答:由于Mg和Mg2+的核内质子数相同,所以两者属于同种元素,S和S2-所带电性不同所以两者属于不同的粒子,由于最外层电子数决定了元素的化学性质,所以由于Na和Na+的最外层电子数分别是1和8,故其化学性质一定不同,原子的质量主要集中在原子核上,而电子的质量很小可以忽略不计,因此Fe2+和Fe3+的原子质量几乎无差别(两者原子核无差别核外电子数不同),所以两者的相对原子质量相同;
故答案为:同种;质子数相同;两种;电性;不同;最外层电子数不同;相同;原子的质量主要集中在原子核上;
点评:此题考查了有关元素的基本概念以及元素的化学性质取决于最外层电子数等知识,考查学生基础知识的掌握能力,难度较小.

练习册系列答案
相关题目
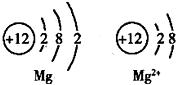 14、如图是Mg和Mg2+的结构示意图,回答下列问题.
14、如图是Mg和Mg2+的结构示意图,回答下列问题.