题目内容
【题目】在宏观、微观与符号之间建立联系,是化学学科的特点。根据下图回答问题。
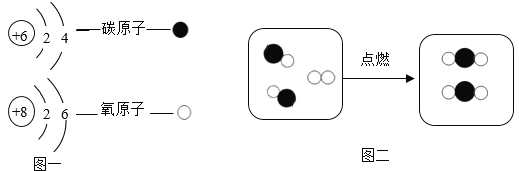
(1)图一中两种微粒属于不同种元素是因为_____不同,用化学符号表示两个碳原子_____
(2)图二中反应的化学方程式为_____,其基本反应类型是_____。
【答案】原子质子数或核电荷数 2C 2CO+O2 2CO2 化合反应
2CO2 化合反应
【解析】
(1)元素是具有相同质子数或核电荷数的一类原子的总称,两种微粒的质子数或核电荷数不同,所以不属于不同种元素;两个碳原子表示为:2C。故填:质子数或核电荷数;2C;
(2)由微观反应示意图可知,该反应是由一氧化碳与氧气在点燃的条件下反应生成二氧化碳,是由两种物质反应生成另一种新物质,符合“多变一”的特征,属于化合反应;故填:2CO+O2 2CO2;化合反应。
2CO2;化合反应。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某小组同学通过资料发现,向不同浓度的碳酸钠和碳酸氢钠溶液中加入氯化钙溶液,会出现以下现象。继而对氯化钙与两种溶液的反应进行了探究。
Na2CO3 | NaHCO3 | |
现象一 | 产生沉淀 | 产生沉淀和气泡 |
现象二 | 产生沉淀 | 产生沉淀 |
现象三 | 产生沉淀 | 无沉淀 |
(查阅资料)
①![]()
②Ca(HCO3)2易溶于水。
(进行实验)
实验一:70℃恒温水浴下,向10 mL不同浓度的Na2CO3和NaHCO3溶液中滴加10%的CaCl2溶液,现象如下表。
浓度 | Na2CO3 | NaHCO3 |
10% | 滴加1滴出现白色沉淀 | 滴加1滴出现白色沉淀,有较多气泡产生 |
5% | 滴加1滴出现白色沉淀 | 滴加1滴出现白色沉淀,30 s后有少量气泡产生 |
1% | 滴加1滴出现白色沉淀 | 滴加10滴出现浑浊 |
0.5% | 滴加1滴出现白色沉淀 | 滴加52滴出现浑浊 |
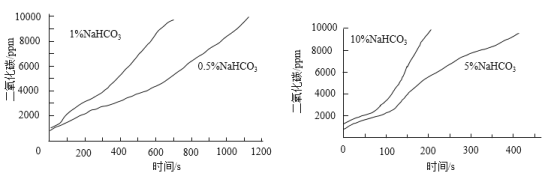
实验二:如图进行实验。70℃恒温水浴下,向10 mL不同浓度的NaHCO3溶液中滴加10%的CaCl2溶液,测得CO2浓度与时间的关系如下图。

(解释与结论)
(1)NaHCO3的俗称是________。
(2)![]() 属于基本反应类型中的________反应。
属于基本反应类型中的________反应。
(3)补全NaHCO3与CaCl2反应的化学方程式:![]() +________+________+H2O。
+________+________+H2O。
(4)实验二得出的结论是________。
(反思与评价)
(5)实验一中,向NaHCO3溶液中滴加CaCl2溶液时,有些只观察到浑浊、未观察到气泡,原因可能是________。
(6)小组同学发现的资料,现象三的NaHCO3溶液中无沉淀,其原因可能为_______。